Artículos originales
Influencia de la anticoncepción sobre la microbiota vaginal
Influence of contraception on the vaginal microbiota
Influencia de la anticoncepción sobre la microbiota vaginal
Bioquímica y Patología Clínica, vol. 89, núm. 2, pp. 15-26, 2025
Asociación Bioquímica Argentina
Resumen: Objetivos: Evaluar el desbalance de la microbiota vaginal, la prevalencia de vaginosis bacteriana (VB), levaduras, trichomoniasis y reacción inflamatoria vaginal (RIV). Caracterizar las especies de lactobacilos en pacientes usuarias de distintos métodos anticonceptivos (preservativos, anticonceptivos orales [ACO], dispositivo intrauterino de cobre [DIU-Cu], ligadura tubaria [LT]). Métodos: Se llevó a cabo un estudio consecutivo, prospectivo y transversal. Se examinaron pacientes de 18 - 50 años. Se realizó examen clínico, estudio de balance del contenido vaginal (BACOVA) y cultivo. La identificación de lactobacilos se hizo por MALDI-TOF. Resultados: Se analizaron 1303 pacientes divididas en grupos: Grupo 1 (G1): ACO (n=314); Grupo 2 (G2): preservativo (n=385); Grupo 3 (G3): DIU-Cu (n=92); Grupo 4 (G4): LT (n=26) y Grupo 5 (G5): control (n=486). La prevalencia de estados vaginales básicos (EVB) de desbalance fue: G1: 34,4% (p=0,18); G2: 42,1% (p=0,12); G3: 48,9% (p=0,05); G4: 53,8% (p=0,14); G5: 37,9%. Los grupos con mayor prevalencia de VB fueron G3: 41,3% (p=0.03) y G4: 50% (p=0,05). Los grupos con mayor prevalencia de levaduras fueron G3: 31,5% (p=0,01) y G4: 38,5% (p=0, 02). El 82,8% (p=0,01) del G3 con levaduras presentó estados inflamatorios (II/V). G3 presentó mayor prevalencia de RIV: 58,7% (p=0,01). L. crispatus tuvo una prevalencia en G1 de 31,6%; en G2 de 25,4%; en G3 de 39,4%; en G4 de 22,2% y en G5 de 29,9%. Conclusión: Se observó mayor desbalance de microbiota, prevalencia de VB y levaduras en usuarias de DIU-Cu. En las usuarias de ACO, predominó el balance de la microbiota y la prevalencia de L. crispatus respecto de las usuarias de barrera y similar al control. Las usuarias de DIU-Cu presentaron mayor RIV por ser un cuerpo extraño.
Palabras clave: anticoncepción, desbalance vaginal, vaginosis bacteriana, levaduras, trichomoniasis, Lactobacillus, reacción inflamatoria.
Abstract: Objectives: To evaluate vaginal dysbiosis, prevalence of bacterial vaginosis (BV), yeasts, trichomoniasis and vaginal inflammatory reaction (VIR), and characterize the lactobacillus species present in patients using different contraceptive methods (oral contraceptive pills (OCPs), condom, Cu-intrauterine device (Cu-IUD) and tubal ligation (TL)). Methods: A cross-sectional, prospective and consecutive study. Patients aged 18-50 years were examined. Clinical examination, balance of vaginal content (BAVACO) study and culture were performed. Lactobacilli were identified by MALDI-TOF. Results: A total of 1303 patients were divided into: Group 1 (G1): OCPs (n=314), Group 2 (G2): Condom (n=385), Group 3 (G3): Cu-IUD (n=92), Group 4 (G4): TL (n=26), and Group 5 (G5): Control (n=486). The prevalence of vaginal dysbiosis was: 34.4% in G1 (p=0.18), 42.1% in G2 (p=0.12), 48.9% in G3 (p=0.05), 53.8% in G4 (p=0.14), and 37.9% in G5. The groups with higher prevalence of BV were G3 (41.3%) (p=0.03) and G4 (50%) (p=0.05). The groups with higher prevalence of yeasts were G3 (31.5%) (p=0.01) and G4 (38.5) (p=0.02). About 82.8% (p=0.01) of G3 patients with yeasts presented inflammatory states (II/V). G3 had higher prevalence of VIR (58.7%) (p=0.01). L. crispatus prevalence was: 31.6% in G1, 25.4% in G2, 39.4% in G3, 22.2% in G4, and 29.9% in G5. Conclusions: Cu-IUD users presented greater vaginal dysbiosis and greater prevalence of BV and yeasts. The microbiota balance and prevalence of L. crispatus predominated in OCP users compared to condom users and were similar to the controls. Cu-IUD users had higher VIR due to the Cu-IUD being a foreign body.
Keywords: contraception, vaginal unbalance, bacterial vaginosis, vaginal yeasts, trichomoniasis, Lactobacillus, vaginal inflammatory reaction.
Introducción
La microbiota vaginal es un complejo sistema de microorganismos relacionados y en permanente equilibrio, que varía a lo largo de la vida. En la pubertad, por el estímulo estrogénico, aumenta el predominio de lactobacilos y, en menor proporción, una gran variedad de especies de bacterias aeróbicas, anaeróbicas y levaduras. Es entonces admisible reconocer la influencia de los estrógenos en la colonización vaginal por lactobacilos1. De esta forma, bajo su acción, el epitelio estratificado aumenta su espesor y los lactobacilos producen ácido láctico como metabolito final de la glucosa2.
Los métodos moleculares demostraron que Lactobacillus crispatus, L. gasseri, L. jensenii y L. iners son los gérmenes más comunes. Sin embargo, el ecosistema vaginal puede ser desequilibrado por una amplia variedad de factores, algunos endógenos y otros exógenos (como la anticoncepción o la terapia de reemplazo hormonal)3.
En la población argentina, de acuerdo con la Encuesta Nacional de Salud Sexual y Reproductiva (ENSSyR), los métodos más utilizados son los hormonales (50,5%) y el preservativo (29,6%). Sin embrago, en el Área Metropolitana de Buenos Aires (AMBA), el 40,2 % de las pacientes utiliza métodos hormonales y el 40%, preservativo4.
El uso de anticonceptivos orales (ACO) se ha asociado con aumento en la abundancia relativa de lactobacilos. Hay datos contradictorios sobre si las especies de lactobacilos que aumentan son protectoras o permisivas con respecto a la vaginosis bacteriana (VB)5. Respecto de los demás métodos anticonceptivos (MAC) -preservativo, dispositivo intrauterino de cobre-DIU-Cu, ligadura tubaria [LT]-, la evidencia es discordante y limitada.
Teniendo en cuenta lo expresado, los objetivos planteados fueron: 1) Evaluar el desbalance de la microbiota vaginal mediante los estados vaginales básicos (EVB) por metodología del balance del contenido vaginal (BACOVA) en usuarias de MAC (preservativos, ACO, DIU-Cu, LT) en comparación con pacientes no usuarias de MAC (control); 2) Evaluar la presencia de patógenos vaginales en usuarias de MAC respecto del control; 3) Evaluar la presencia de reacción inflamatoria vaginal (RIV) en usuarias de MAC respecto del control; 4) Caracterizar las especies de lactobacilos asociadas a usuarias de distintos MAC.
Materiales y métodos
Se realizó un estudio observacional, analítico, consecutivo, prospectivo, de corte transversal. Se examinaron pacientes entre 18 y 50 años, con inicio de relaciones sexuales y ciclos menstruales conservados, atendidas entre enero del 2013 y diciembre del 2022. Este trabajo fue aprobado por el Comité de Ética del hospital, y todas las pacientes dieron su consentimiento informado.
Población
Criterios de inclusión: pacientes entre 18 y 50 años, con inicio de relaciones sexuales, ciclos menstruales conservados, usuarias de MAC (preservativo, ACO, anticonceptivos inyectables, implante subdérmico, SIU-LNG (levonorgestrel), DIU-Cu, coitus interruptus, anillo vaginal, LT. Grupo control: no usuarias de MAC.
Criterios de exclusión: uso de antibióticos (ATB) locales o sistémicos, embarazadas, malformaciones genitales, pacientes en tratamiento con corticoides o quimioterapia, pacientes que no tuvieran abstinencia sexual dentro de las 48 h previas al estudio. Criterios de eliminación: grupo de estudio cuyo número muestral fuera menor de 10.
Metodología
Luego de la firma del consentimiento informado, se procedió a la recolección de datos para completar la ficha ginecológica. Además, se recogieron datos médicos y epidemiológicos de interés. A todas las pacientes se les realizó examen clínico y toma de fondo de saco vaginal para el estudio microbiológico por metodología convencional y estudio de los EVB mediante BACOVA.
- 1.
1. Extendidos para coloración de Gram y May-Grünwald Giemsa prolongado;
2. Observación en fresco con 1 ml de solución fisiológica (SF);
3. Determinación de pH de la secreción vaginal;
4. Observación en fresco con 1 ml de KOH al 10% y prueba de aminas;
5. Cultivo en medio líquido (tioglicolato modificado) para Trichomonas vaginalis, con incubación de 7 días a 37oC en atmósfera de 5 % de CO26;
6. Cultivo en agar base Columbia con 5% de sangre humana y en agar Man-Rogosa-Sharpe con incubación de 48 h a 37°C en atmósfera de 5% de CO2, conservando la muestra en medio de Stuart.
La detección de levaduras se realizó a través de la observación en fresco con SF y con KOH al 10 % y por cultivo en agar Sabouraud y agar sangre.
La investigación de T. vaginalis se llevó a cabo a través de la observación microscópica directa con SF, la coloración de May-Grünwald, Giemsa prolongado y el cultivo en tioglicolato modificado6,7. El diagnóstico de VB se realizó utilizando el criterio de Nugent8.
El estudio del BACOVA incluyó el análisis morfológico del contenido vaginal en función de la relación del valor numérico (VN) y RIV, y se identificaron 5 EVB: microbiota normal (I), microbiota normal más reacción inflamatoria (II), microbiota intermedia (III), VB (IV) y vaginitis microbiana inespecífica (V) (Fotos 1)9.
Para el aislamiento de las distintas especies de lacobacilos, se utilizaron el agar sangre y el agar Man-Rogosa, y la identificación se realizó mediante espectrometría de masa BDTM Bruker MALDI-TOF (desorción/ionización láser asistida por matriz, con detector de iones por tiempo de vuelo), utilizando una base de datos que incluyó más de 90 especies de lactobacilos y considerando un score ≥ 1,7 para nivel de especie, método validado contra la secuenciación del gen ADNr 16S (método de referencia)(Foto 2)10,11,12.
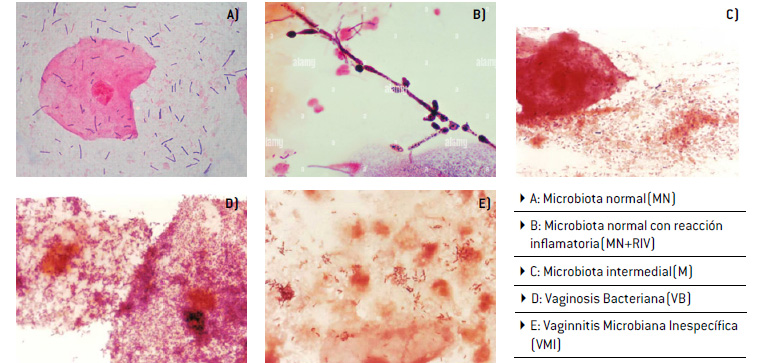
Foto 1
Estados vaginales básicos (EVB): observación en la coloración de Gram (1000X) del contenido vaginal
Una captura de un celular con texto e imágenes, descripción generada automáticamente con confianza baja.
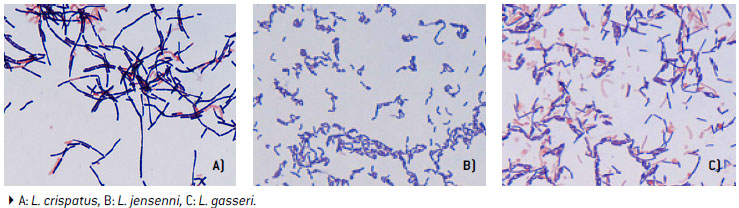
Foto 2
Morfología de Lactobacillus spp.: observación en la coloración de Gram (1000X)
Dibujo en blanco y negro, el contenido generado por IA puede ser incorrecto.
Análisis de datos
Para comparar las prevalencias de los EVB, de levaduras, VB, trichomoniasis y de las especies de lactobacilos, en los distintos grupos de MAC respecto del control, se utilizaron el test de Chi cuadrado (χ2) y el test de Fisher. Se consideró significativo un valor de p menor de 0,05.
Resultados
De las 1326 pacientes, se excluyeron 23 por el bajo número muestral, que utilizaban: anticoncepción inyectable (9), SIU-LNG (6), implante hormonal (6), coitus interruptus (1) y anillo vaginal (1). Se analizaron las restantes 1303 pacientes, divididas en 4 grupos: Grupo 1, ACO, (n=314); Grupo 2, preservativo, (n=385); Grupo 3, DIU-Cu, (n=92); Grupo 4, LT, (n=26), Grupo 5, control, (n=486).
En la Tabla I, se observan los MAC utilizados en nuestra población. Lo más frecuente fue la no utilización de MAC: 36,6% (486/1326), seguida de preservativo: 29,1% (385/1326) y ACO: 23,7% (314/1326).
La prevalencia de EVB de desbalance vaginal (III, IV y V) fue: Grupo 1: 34,4% (OR: 0,86 IC95% 0,64-1,16 p=0,18); Grupo 2: 42,1% (OR 1,19 IC95% 0,91-15,57 p=0,12); Grupo 3: 48,9% (OR 1,57 IC95% 1,00-2,46 p=0,05); Grupo 4: 53,8% (OR 1,91 IC95% 0,87-4,22 p=0,14); Grupo 5: 37,9% (Tabla II).
La prevalencia de VB en los distintos MAC respecto del control fue la siguiente: Grupo 1: 29% (OR: 0,9 IC95% 0,66-1,23 p=0,52); Grupo 2: 37,4% (OR 1,32 IC95% 1,0-1,75 p=0,06); Grupo 3: 41,3% (OR 1,56 IC95% 0,98-2,46 p=0,03); Grupo 4: 50% (OR 2,21 IC95% 1,0-4,88 p=0,05); Grupo 5: 31,1%. El análisis de prevalencia de levaduras en los distintos MAC respecto del control fue: Grupo 1: 21,3% (OR: 1,11 IC95% 0,78-1,58 p=0,3); Grupo 2: 21,8% (OR 0,82 IC95% 0,82-1,6 p=0,23); Grupo 3: 31,5% (OR 1,89 IC95% 1,15-3,1 p=0,01); Grupo 4: 38,46% (OR 2,56 IC95% 1,13-5,83 p=0,02); Grupo 5: 19,6%. El análisis de prevalencia de trichomoniasis en los distintos MAC respecto del control fue: Grupo 1: 3,5% (OR: 0,76 IC95% 0,36-1,6 p=0,3); Grupo 2: 4,4% (OR 0,97 IC95% 0,51-1,86 p=0,53); Grupo 3: 2,2% (OR 0,47 IC95% 0,11-2,02 p=0,23); Grupo 4: 7,7% (OR 1,75 IC95% 0,39-7,9 p=0,34); Grupo 5: 4,5%. (Tabla III).
El análisis de prevalencia de RIV (Estados II/V) en los distintos grupos de MAC respecto del control fue: Grupo 1: 44,9% (OR 0,98 IC95% 0,74-1,31 p=0,48); Grupo 2: 46,5% (OR 1,05 IC95% 0,87-1,37 p=0,38); Grupo 3: 58,7% (OR 1,71 IC95% 1,09-2,7 p=0,01); Grupo 4: 42,3% (OR 0,88 IC95% 0,4-1,97 p=0,46); Grupo 5: 45,4%. (Tabla IV).
En la Tabla V, se observa la prevalencia de EBV con RIV (II/V) en pacientes con levaduras; según el MAC, respecto del control, fue la siguiente: Grupo 1: 64,2% (OR 1,41 IC95% 0,75-2,7 p=0,18); Grupo 2: 54,8% (OR 0,95 IC95% 0,53-1,73 p=0,5); Grupo 3: 82,8% (OR 3,8 IC95% 1,34-10,82 p=0,01); Grupo 4: 70% (OR 1,85 IC95% 0,45-7,59 p=0,3); Grupo 5: 55,8%.
Se detectó microbiota lactobacilar en 790 pacientes (Grupo 1: 206; Grupo 2: 223; Grupo 3: 48; Grupo 4: 12; Grupo 5: 301), y se caracterizaron 440 lactobacilos cultivables. L. crispatus tuvo una prevalencia en Grupo 1 del 31,6%, en Grupo 2: 25,4%, en Grupo 3: 39,4%, en Grupo 4: 22,2% y en Grupo 5: 29,9% (Tabla VI). Se detectó asociación positiva de este germen en el Grupo 1 respecto del Grupo 2; OR 1,36 (IC95% 0,78-2,37) y similar prevalencia respecto del control: OR 1,08 (IC95% 0,64-1,83).
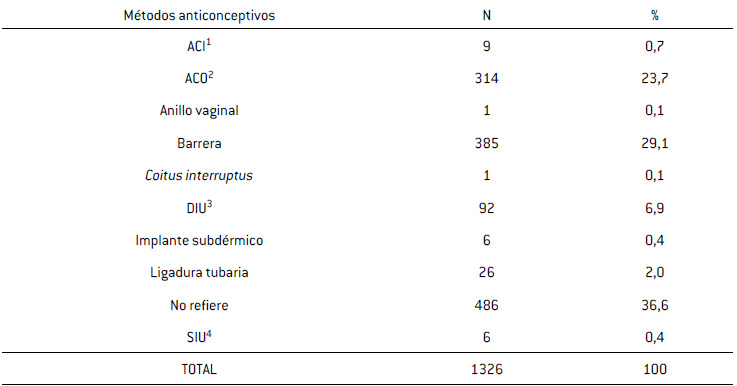
Tabla I
Métodos anticonceptivos usados en la población estudiada
1ACI, Anticonceptivo Inyectable; 2ACO, Anticonceptivo Oral; 3DIU, Dispositivo Intrauterino; 4SIU[DM1] , Sistema Intrauterino.
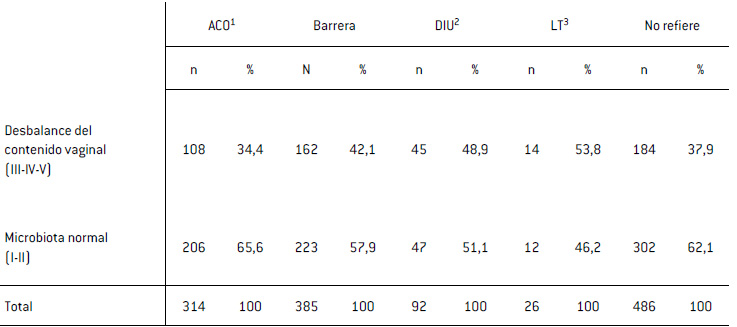
Tabla II
Prevalencia de los estados vaginales básicos (EVB) de desbalance del contenido vaginal según método anticonceptivo
1ACO, Anticonceptivo oral: 2DIU, Dispositivo intrauterino; 3LT, Ligadura tubaria.
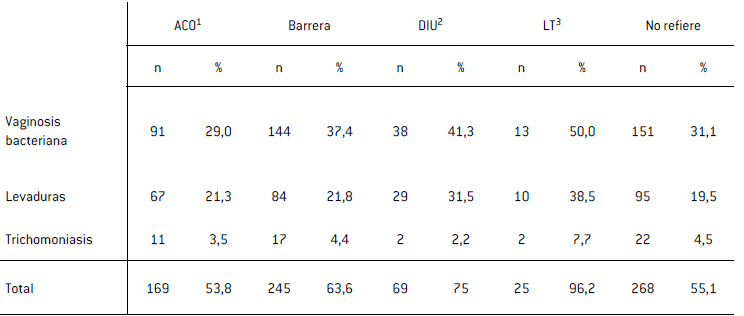
Tabla III
Prevalencia de vaginosis bacteriana, levaduras y trichomoniasis el método anticonceptivo
1ACO, Anticonceptivo oral: 2DIU, Dispositivo intrauterino; 3LT, Ligadura tubaria.
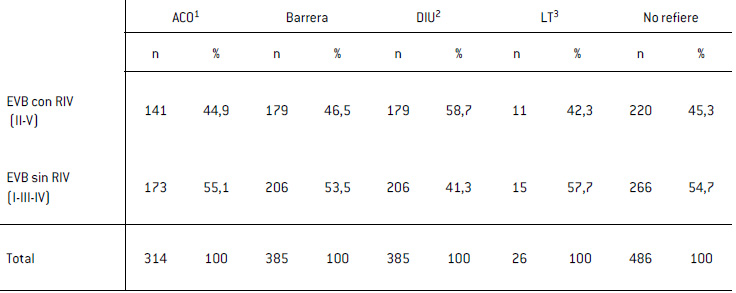
Tabla IV
Prevalencia de los estados vaginales básicos (EVB) con reacción inflamatoria vaginal (RIV) según método anticonceptivo
1ACO, Anticonceptivo oral: 2DIU, Dispositivo intrauterino; 3LT, Ligadura tubaria.
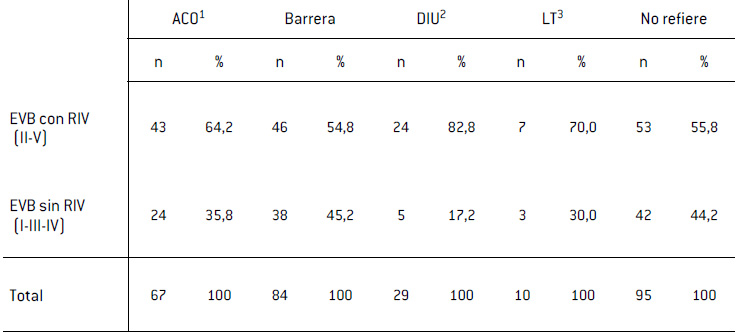
Tabla V
Prevalencia de los estados vaginales básicos (EVB) con reacción inflamatoria vaginal (RIV)en pacientes con levaduras según método anticonceptivo
1ACO, Anticonceptivo oral: 2DIU, Dispositivo intrauterino; 3LT, Ligadura tubaria.
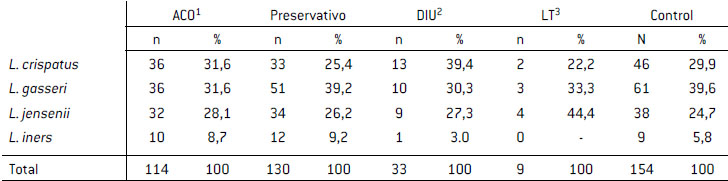
Tabla VI
Prevalencia de las diferentes especies de lactobacilos halladas en los pacientes de acuerdo con el método anticonceptivo
1ACO, Anticonceptivo oral: 2DIU, Dispositivo intrauterino; 3LT, Ligadura ubaria.
Discusión
Según nuestro estudio, el 36,6% de las pacientes no utilizó MAC. Según la ENSSyR, las mujeres informan que las principales razones para no usar MAC son el embarazo actual o el deseo de quedar embarazada4.
En nuestra casuística, el MAC más frecuente fue el preservativo (29,1%), seguido del ACO (23,7%). En la población argentina, los métodos más utilizados son los hormonales (50,5%) y el preservativo, que le sigue en frecuencia (29,6%). Sin embrago, en el AMBA, el 40,2 % de las pacientes utiliza métodos hormonales y el 40%, preservativo4.
Acorde con esta investigación, en las usuarias de ACO, predominó el balance de la microbiota (EVB I: 36,3% y EVB II: 29,3%). Estos resultados coinciden con otros estudios que hacen referencia a la relación estable entre el uso de ACO y la reducción en la prevalencia de VB (EVB IV)13. Vodstrcil et al.14 demostraron un riesgo significativamente reducido de prevalencia, incidencia y recurrencia de VB en usuarias de ACO. Esto puede deberse a que el estrógeno induce la acumulación de glucógeno en el epitelio vaginal, lo que influye en la colonización por lactobacilos que protegen contra la disbiosis (EVB IV y V)15.
En nuestra casuística, la prevalencia de levaduras en usuarias de ACO fue de 21,3%, 64,2% en EVB con RIV (II-V) y 35,8% en EVB sin RIV (I-III-IV). Esto concuerda con los resultados de la Red Nacional BACOVA, que describe un aumento en la frecuencia de levaduras en usuarias de ACO, asociadas a EVB con RIV (II-V) 69,7%16.
La exposición a ACO produce aumento del glucógeno epitelial, reduce la infiltración por leucocitos y la actividad antifúngica del epitelio. Estos cambios garantizan una buena concentración de lactobacilos, pero podrían explicar la presencia de levaduras en cultivos de mujeres usuarias de ACO17,18. Además de estos efectos sobre el huésped, el estrógeno promueve respuestas adaptativas en Candida spp. que inducen la evasión del sistema inmunitario innato a través de la inhibición de opsonización mediada por complemento dependiente de Gpd2. Además, los estrógenos inician la metaplasia del epitelio columnar a epitelio escamoso estratificado favoreciendo la adherencia y promoviendo el crecimiento de C. albicans19.
Conforme con este estudio, el 3,5% de usuarias de ACO presentó trichomoniasis. Resultados similares fueron observados por Brahmbhatt et al.20, quienes reportan una prevalencia del 4,0%.
Asimismo, se encontró en nuestro estudio 31,6% de L. crispatus en las pacientes usuarias de ACO en comparación con las usuarias de barrera y similar prevalencia respecto del control, en consonancia con Brooks et al.21, quienes refieren que las mujeres usuarias de ACO incrementan la colonización por especies de lactobacilos productoras de agua oxigenada, como L. crispatus.
En nuestra cohorte, se observó un 42,1% de desbalance de la microbiota vaginal en las usuarias de preservativo. Belchior et al.16relatan que el preservativo masculino se asoció positivamente con VB (OR 1,34; IC95% 1,12-1,60), mientras que Bradshaw et al.22 observaron que el preservativo tiene un comportamiento dual sobre la presencia de VB dependiendo de la utilización correcta (previo a que toque la boca o la zona genital de la pareja sexual). Según este estudio, el uso correcto presentó una asociación negativa con VB de 0,96 (IC95% 0,64-1,43), mientras que el uso incorrecto mostró una asociación positiva con VB de 1,96 (IC95% 1,29-2,99). Resultados similares fueron obtenidos en nuestro estudio, que evidenció una asociación con VB de 1,32 (IC95% 1,0-1,75), sin embargo, no se tomó en cuenta la utilización correcta o incorrecta del mismo. En contraposición, el estudio transversal de Hitchcock et al.23 demostró que el uso de preservativo se asociaba con una disminución en el riesgo de VB.
Un estudio que analizó la distribución de levaduras en usuarias de distintos MAC encontró que las pacientes que utilizaban preservativo tuvieron una asociación menor con infección sintomática por Candida spp. respecto de ACO24. En este mismo sentido, nuestros datos reportan que las pacientes que utilizaban el preservativo como MAC tuvieron un OR de 1,14 (IC95% 0,82-1,6).
Está bien documentado el efecto protector del preservativo frente a trichomoniasis, al evitar el contacto de secreciones23. En una revisión sistemática, se observó una baja tasa de infección por trichomoniasis entre las usuarias de preservativo, mientras que, en otros estudios, no se vio la asociación25.
Ma et al.5 relacionaron el uso constante de preservativos con el aumento de la colonización por L. crispatus y la protección contra la VB y HIV. En nuestra casuística, el 25,4% de las pacientes que utilizaron método de barrera tuvieron colonización por L. crispatus.
El 48,9% de las usuarias de DIU-Cu tuvieron desbalance de la microbiota. Belchior et al.16 refieren su asociación con el desbalance de la microbiota vaginal tanto en el EVB IV (OR 1,32 IC95% 0,98-1,76) como en el EVB V (OR 2,34 IC95% 1,74-3,12). Este desbalance podría explicarse porque, al representar un cuerpo extraño que permanece largos períodos de tiempo, se modifica el ecosistema vaginal. Asimismo, nuestro estudio detectó 41,3% de VB en usuarias de DIU-Cu. Un estudio longitudinal estimó la prevalencia asintomática de VB demostrando un aumento en mujeres que iniciaron el DIU-Cu del 27 % al inicio al 35 % a los 30 días, al 40 % a los 90 días y al 49 % a los 180 días13. También reportaron mayor colonización por G. vaginalis y A. vaginae13.
Este estudio describió, además, un aumento de la prevalencia de levaduras en usuarias de DIU-Cu de 31,5%, con un predominio de estados inflamatorios (82,8%). En coincidencia con estos resultados, algunos estudios encontraron que la incidencia de colonización y vulvovaginitis por Candida spp. es mayor entre las usuarias de DIU-Cu26,27,28. Se ha sugerido que la asociación del uso del DIU-Cu con episodios de vulvovaginitis se debe a la adhesión de las levaduras y la formación de biopelícula. Una biopelícula es una comunidad de microorganismos asociados a la superficie, inmersos en una matriz extracelular de producción que confiere resistencia a los antifúngicos, la inmunidad del huésped y el estrés. Las levaduras pueden formar biopelículas en las superficies inertes de varios dispositivos implantados, incluidos catéteres, válvulas cardíacas protésicas y DIU-Cu29,30.
La prevalencia de trichomoniasis en nuestra serie fue de 2,2% en usuarias de DIU-Cu. Estas cifras son menores que las referidas en un estudio de Uganda en donde se comunicaron tasas más altas de T. vaginalis entre las usuarias de DIU-Cu30. Existe poca evidencia sobre esta asociación, aunque probablemente pueda deberse al aumento del sangrado menstrual asociado al DIU-Cu de cobre, que favorecería la supervivencia del parásito. Otro posible mecanismo causal son los cambios de desbalance de la microbiota que genera el DIU-Cu31,32.
Nuestros resultados describen en las pacientes usuarias de DIU-Cu un incremento significativo de los EVB con RIV (58,7%). Hallazgos similares fueron referidos por un estudio que evaluó los resultados citológicos de usuarias de DIU-Cu y constató que la infiltración inflamatoria fue significativamente más frecuente en los grupos SIU-LNG (54,9 %) y DIU (57,2 %) que en el grupo control (50,2 %)33.
En nuestra casuística, se reportó una prevalencia de L. crispatus de 39,4% en usuarias de DIU-Cu. Bassis et al.34 han llevado a cabo una comparación de los efectos de la anticoncepción intrauterina en la microbiota vaginal describiendo que la microbiota vaginal estaba agrupada en tres comunidades bacterianas vaginales principales: una, dominada por L. iners; otra, por L. crispatus y una no dominada por ningún lactobacilo. Cuando se examinó la microbiota a los 6 meses de utilización de DIU-Cu, se advirtieron 2 extremos en la estabilidad: las comunidades altamente estables, dominadas por L. iners en las pacientes usuarias de SIU-LNG, y las comunidades no dominadas por lactobacilos en las pacientes usuarias de DIU-Cu, relacionadas con disbiosis.
La LT es un método de anticoncepción quirúrgico permanente para mujeres. No existen prácticamente datos sobre su influencia en el desbalance de la microbiota vaginal. En nuestra investigación, se detectó un incremento en la prevalencia de VB (50%) y de levaduras (38,5%) en las pacientes con LT. De manera similar, el estudio realizado por Riggs et al.35 en pacientes con LT mostró VB en la mayoría de sus casos (66%).
Nuestro estudio detectó una prevalencia de 7,7% de infección por T. vaginalis en las pacientes con LT. Sin embargo, según los datos proporcionados por Nikpay et al.36, las pacientes que utilizaron la LT como método anticonceptivo tuvieron prevalencias mayores de trichomoniasis.
En nuestra casuística, relatamos una prevalencia de 42,3% de estados con RIV (Estados II/V) en las pacientes con LT. Resultados similares fueron descriptos por Garg et al.37 en India, quienes describieron que la RIV de las pacientes sometidas a LT estuvo presente en el 41%.
Conclusiones
En conclusión, se observó mayor desbalance de la microbiota vaginal en las pacientes usuarias de DIU-Cu respecto del control. En cambio, en las usuarias de ACO, predominó el balance de la microbiota por el aporte hormonal. Se observó también mayor prevalencia de VB en las pacientes usuarias de DIU-Cu y tendencia en las usuarias de preservativo y LT respecto del control. Se detectó mayor prevalencia de levaduras en el grupo de DIU-Cu y de LT, sin embargo, el DIU-Cu fue el único método en donde este microorganismo se asoció a RIV. No se observaron diferencias significativas en las prevalencias de trichomoniasis en los distintos grupos de estudio. También se observó que las usuarias de DIU-Cu presentaron una mayor RIV que el control, por ser un cuerpo extraño. Las usuarias de ACO tuvieron mayor prevalencia de L. crispatus (especie protectora), cuando se las comparó con las usuarias de barrera, y similar prevalencia con el grupo control.
Agradecimientos
El presente trabajo ha sido financiado por el Proyecto UBACYT-20020150200194BA de la Universidad de Buenos Aires (UBA).
Referencias bibliográficas
1. Petricevic L, Domig KJ, Nierscher FJ, Krondorfer I, Janitschek C, Kneifel W, et al. Characterization of the oral, vaginal and rectal Lactobacillus flora in healthy pregnant and postmenopausal women. Europ J Obstet Gynecol Reprod Biol 2012;160(1):93-9, https://doi.org/10.1016/j.ejogrb.2011.10.002
2. Cauci S, Driussi S, De Santo D, Penacchioni P, Iannicelli T, Lanzafame P, et al. Prevalence of bacterial vaginosis and vaginal flora changes in peri- and postmenopausal women. J Clin Microbiol 2002; 40(6):2147-2, https://doi.org/10.1128/JCM.40.6.2147-2152.2002
3. Behbakht K, Friedman J, Heimler I, Aroutcheva A, Simoes J, Faro S. Role of the vaginal microbiological ecosystem and cytokine profile in the promotion of cervical dysplasia: a case-control study. Infect Dis Obstet Gynecol 2002;10(4):181-6, https://doi.org/10.1155/S1064744902000200
4. Ministerio de Salud de la Nación Argentina (2013). Encuesta Nacional sobre Salud Sexual y Reproductiva. Documento de Trabajo N° 1: Acceso y uso de métodos anticonceptivos. Mujeres de 14 a 49 años.
5. Ma L, Lv Z, Su J, Wang J, Yan D, Wei J, et al. Consistent condom use increases the colonization of Lactobacillus crispatus in the vagina. PloS one 2013; 8(7): e70716, https://doi.org/10.1371/journal.pone.0070716
6. Poch F, Levin D, Levin S, Dan M. Modified thioglycolate medium: a simple and reliable means for detection of Trichomonas vaginalis. J Clin Microbiol 1996; 34(10): 2630-1, https://doi.org/10.1371/journal.pone.0070716
7. Perazzi BE, Menghi CI, Coppolillo EF, Gatta C, Eliseth MC, de Torres RA, et al. Prevalence and comparison of diagnostic methods for Trichomonas vaginalis infection in pregnant women in Argentina. Korean J Parasitol 2010; 48(1):61-5, https://doi.org/10.3347/kjp.2010.48.1.61
8. Nugent RP, Krohn MA, Hillier SL. Reliability of diagnosing bacterial vaginosis is improved by a standardized method of gram stain interpretation. J Clin Microbiol. 1991;29(2):297-301, https://doi.org/10.1128/jcm.29.2.297-301.1991
9. Proyecto BACOVA, Programa PROSAR, Fundación Bioquímica Argentina. Manual de Procedimientos BACOVA 2018. Disponible en: http://www. fba.org.ar/PROSAR Discusión LTB file:///C:/Users/Usuario/Downloads/
10. Jorgensen JH, Pfaller MA, Carrol KC, Funke G, Landry ML, Richter SS, Warnock DW, editors. Manual of Clinical Microbiology. 11th edition. Washington DC, ASM Press, 2015.
11. Karas M, Krger R. Ion Formation in MALDI: The Cluster Ionization Mechanism. Chemical Reviews 2003; 103: 427440, https://doi.org/10.1021/cr010376a
12. Pavlova SI, Kilic AO, Kilic SS, SO JS, Nader-Macias ME, Simoes JA, et al. Genetic diversity of vaginal lactobacilli from women in different countries on 16S rRNA gene sequences. J Appl Microbiol 2002; 92:451-9, https://doi.org/10.1046/j.1365-2672.2002.01547.x
13. Achilles SL., Austin MN., Meyn LA., Mhlanga F., Chirenje ZM, Hillier SL. Impact of contraceptive initiation on vaginal microbiota. Am J Obstet Gynecol 2018:218(6),622.e1-622.e10, https://doi.org/10.1016/j.ajog.2018.02.017
14. Vodstrcil LA, Hocking JS, Law M, Walker S, Tabrizi SN, Fairley CK, et al. Hormonal contraception is associated with a reduced risk of bacterial vaginosis: a systematic review and meta-analysis. PloS one 2013; 8(9):e73055, https://doi.org/10.1371/journal.pone.0073055
15. Fosch SE, Ficoseco CA, Marchesi A, Cocucci S, Nader-Macias MEF, Perazzi BE. Contraception: Influence on Vaginal Microbiota and Identification of Vaginal Lactobacilli Using MALDI-TOF MS and 16S rDNA Sequencing. Open Microbiol J 2018;12:218-29, https://doi.org/10.2174/1874285801812010218
16. Belchior S Fosch S, Yones C, de Torres R, Palaoro L, Micucci H, et al. Estudio multicéntrico de disfunción vaginal de la Red Nacional de Laboratorios BACOVA de la República Argentina: prevalencia, influencia de factores seleccionados, evaluación clínica y distribución de casos por región. Acta Bioq Clin Latin 2021; 55(Supl. 1):49-50.
17. van de Wijgert JH, Verwijs MC, Turner AN, Morrison CS. Hormonal contraception decreases bacterial vaginosis but oral contraception may increase candidiasis: implications for HIV transmission. AIDS (London, England), 2013; 27(13):2141-53.
18. Mishell DR, Jr, el-Habashy MA, Good RG, Moyer DL. Contraception with an injectable progestin. A study of its use in postpartum women. Am J Obstet Gynecol 1968;101(8):1046-53, https://doi.org/10.1097/QAD.0b013e32836290b6
19. Kumwenda P, Cottier F, Hendry AC, Kneafsey D, Keevan B, Gallagher H, et al Estrogen promotes innate immune evasion of Candida albicans through inactivation of the alternative complement system. Cell Rep2022;38(1):110183, https://doi.org/10.1016/j.celrep.2021.110183
20. Brahmbhatt H, Musoke R, Makumbi F, Kigozi G, Serwadda D, Wawer M, et al. Trichomonas vaginalis Incidence Associated with Hormonal Contraceptive Use and HIV Infection among Women in Rakai, Uganda. J Sex Trans Dis, 2014; 916597, https://doi.org/10.1155/2014/916597
21. Brooks JP, Edwards DJ, Blithe DL, Fettweis JM, Serrano MG, Sheth NU, et al. Effects of combined oral contraceptives, depot medroxyprogesterone acetate and the levonorgestrel-releasing intrauterine system on the vaginal microbiome. Contraception 2017;95(4):405-13, https://doi.org/10.1016/j.contraception.2016.11.006
22. Bradshaw CS, Vodstrcil LA, Hocking JS. Law M, Pirotta M, Garland S M., et al. Recurrence of bacterial vaginosis is significantly associated with posttreatment sexual activities and hormonal contraceptive use. Clin Infect Dis 2013;56(6):777-86, https://doi.org/10.1093/cid/cis1030
23. Hitchcock P. Scientific evidence on condom effectiveness for sexually transmitted disease (STD) prevention: workshop summary. Herndon (Va): Diane Publishing, 2001, p.12-3.
24. Cetin M, Ocak S, Gungoren A, Hakverdi AU. Distribution of Candida species in women with vulvovaginal symptoms and their association with different ages and contraceptive methods. Scand J Infect Dis 2007;39(6-7):584-8, https://doi.org/10.1080/00365540601148491
25. Arbabi M, Delavari M, Fakhrieh-Kashan Z, Hooshyar H. Review of Trichomonas vaginalis in Iran, Based on Epidemiological Situation. J Reprod Infert 2018; 19(2):82-8.
26. Apalata T, Longo-Mbenza B, Sturm A, Carr W, Moodley P. Factors Associated with Symptomatic Vulvovaginal Candidiasis: A Study among Women Attending a Primary Healthcare Clinic in Kwazulu-Natal, South Africa. Ann Med Health Sci Res2014;4(3):410-6, https://doi.org/10.4103/2141-9248.133470
27. Borges KRA, Pimentel IV, Lucena LCLDS, Silva MACND, Monteiro SG, Monteiro CA, et al. Adhesion and biofilm formation of Candida parapsilosis isolated from vaginal secretions to copper intrauterine devices. Rev Inst Med Trop Sao Paulo 2018;60:e59, https://doi.org/10.1590/S1678-9946201860059
28. Demirezen S, Dirlik OO, Beksaç MS. The association of Candida infection with intrauterine contraceptive device. Cent Eur J Public Health2005;13(1):32-4.
29. Gonçalves B, Ferreira C, Alves CT, Henriques M, Azeredo J, Silva S. Vulvovaginal candidiasis: Epidemiology, microbiology and risk factors. Crit Rev Microbiol 2016;42(6):905-27, https://doi.org/10.3109/1040841X.2015.1091805
30. Lohse MB, Gulati M, Johnson AD, Nobile CJ. Development and regulation of single- and multi-species Candida albicans biofilms. Nat Rev Microbiol 2018; 16(1):19-31, https://doi.org/10.1038/nrmicro.2017.107
31. Kiweewa FM, Brown E, Mishra A, Nair G, Palanee-Phillips T, Mgodi N, et al. MTN-020/ASPIRE Study Team. Acquisition of Sexually Transmitted Infections among Women Using a Variety of Contraceptive Options: A prospective Study among High-risk African Women. J Int AIDS Soc 2019; 22(2):e25257, https://doi.org/10.1002/jia2.25257
32. Ryu JS, Choi HK, Min DY, Ha SE, Ahn MH. Effect of iron on the virulence of Trichomoniasis vaginalis. J Parasitol 2001; 87(2):457-60, https://doi.org/10.1645/0022-3395(2001)087[0457:EOIOTV]2.0.CO;2
33. Eleuterio J, Junior Giraldo PC, Silveira Gonçalves AK, Nunes Eleuterio RM. Liquid-based cervical cytology and microbiological analyses in women using cooper intrauterine device and levonorgestrel-releasing intrauterine system. Eur J Obstet Gynecol Reprod Biod 2020; 255:20-4, https://doi.org/10.1016/j.ejogrb.2020.09.051
34. Bassis CM, Allsworth JE, Wahl HN, Sack DE, Young VB, Bell JD. Effects of intrauterine contraception on the vaginal microbiota. Contraception 2017; 96(3):189-95, https://doi.org/10.1016/j.contraception.2017.05.017
35. Riggs M, Klebanoff M, Nansel T, Zhang J, Schwebke J, Andrews W. Longitudinal association between hormonal contraceptives and bacterial vaginosis in women of reproductive age. Sex Trans Dis 2007; 34(12):954-9.
36. Nikpay S, Otaghi M, Azami M, Karimi M, Abdi J. Trichomonas vaginalis Infection Among Women Attending Laboratory Centers in Ilam, Iran. Infect Disord Drug Targets 2020; 20(1):98-101, https://doi.org/10.2174/1871526519666190117120705
37. Garg K, Khare A, Bansal R, Sharma S, Chaudhary N. Effects of Different Contraceptive Methods on Cervico-Vaginal Cytology. J Clin Diagn Res 2017; 11(7): EC09-EC11, https://doi.org/10.7860/JCDR/2017/28213.10219
Notas
Notas de autor
beatrizperazzi@gmail.com
Información adicional
redalyc-journal-id: 651

