Artículos originales
Ferroptosis, un mecanismo de muerte celular presente en β-talasemia menor
Ferroptosis, a cell death mechanism present in β-thalassemia minor
Ferroptosis, un mecanismo de muerte celular presente en β-talasemia menor
Bioquímica y Patología Clínica, vol. 89, núm. 1, pp. 19-26, 2025
Asociación Bioquímica Argentina
Resumen: Introducción: La ferroptosis es un tipo de muerte celular programada, dependiente de hierro, impulsada por una severa peroxidación lipídica, la cual es consecuencia del metabolismo celular y de una homeostasis redox desequilibrada. La β-talasemia es una anemia hereditaria que cursa con eritropoyesis ineficaz y hemólisis, cuya complicación más importante es la sobrecarga de hierro. Objetivos: Identificar y caracterizar proteínas de la membrana eritrocitaria implicadas en la ferroptosis en pacientes con rasgo β-talasémico (RBT). Materiales y Métodos: Se estudió el proteoma de membranas de eritrocitos desprovistos de hemoglobina de 4 sujetos RBT (grupo RBT) y 4 sujetos control por HPLC acoplado a espectrometría de masa. El análisis e identificación de proteínas se realizó empleando Proteome Discoverer V1.4, y el software Perseus para su cuantificación. Se utilizó la plataforma BlastKOALA para la caracterización funcional de cada proteína. Resultados: Se encontró que las proteínas PCBP 1 y 2 (chaperonas del hierro que favorecen su depósito), P67 y P40 (subunidades catalíticas de la NADPH oxidasa) y ALOX15 (marcadora de peroxidación lipídica), proteínas involucradas en la vía ferroptótica, aumentaron significativamente en el grupo RBT (p<0,05), y su abundancia fue 3,1; 4,4; 3,3; 4,7 y 3 veces mayor que en el grupo control, respectivamente. Conclusiones: La sobreexpresión de proteínas implicadas en la ferroptosis en portadores de β-talasemia avala la participación de este tipo de muerte celular no apoptótica en la fisiopatología de esta anemia hereditaria.
Palabras clave: ferroptosis, β-talasemia, hierro, estrés oxidativo.
Abstract: Introduction: Ferroptosis is an iron (Fe)-dependent programmed cell death driven by severe lipid peroxidation, which is a consequence of cell metabolism and imbalanced redox homeostasis. β-thalassemia is a hereditary anemia that causes ineffective erythropoiesis and hemolysis, with iron overload being its most important complication. Objectives: The purpose of the study was to identify and characterize erythrocyte membrane proteins involved in ferroptosis in patients with β-thalassemia trait (BTT). Materials and Methods: The proteome of hemoglobin-depleted erythrocyte membranes from four BTT subjects and four control subjects was examined by HPLC coupled to mass spectrometry. Proteins were analyzed and identified using Proteome Discoverer V1.4 and quantified using the Perseus software. The BlastKOALA platform was used to characterize each protein functionally. Results: The following ferroptotic pathway proteins were significantly increased in the BTT group (p<0.05): PCBP 1 and 2 (iron chaperones that favor its deposition), P67 and P40 (NADPH oxidase catalytic subunits), and ALOX15 (lipid peroxidation marker), whose abundance was 3.1 and 4.4, 3.3 and 4.7, and 3 times higher than in the control group, respectively. Conclusions: The overexpression of proteins involved in ferroptosis in BTT carriers supports the contribution of this non-apoptotic cell death to β-thalassemia pathophysiology.
Keywords: ferroptosis, β-thalassemia, iron, oxidative stress.
Introducción
La beta (β)-talasemia se caracteriza por una síntesis reducida de la subunidad β de hemoglobina, que produce anemia microcítica hipocrómica y cantidades reducidas de hemoglobina A (HbA). La disminución o ausencia del número de cadenas β produce un exceso relativo de cadenas alfa (α). Las α- globinas libres forman agregados que se autooxidan, desnaturalizan y precipitan como hemicromos en los eritroblastos talasémicos. Como resultado, se generan especies reactivas de oxígeno (ERO), así como grupo hem y hierro en su forma libre. Las ERO, que también son producidas a partir del hierro libre mediante la reacción de Fenton, oxidan lípidos, ácidos nucleicos y proteínas celulares. La evidencia existente sugiere claramente que el exceso de cadenas de α- globina libres es directamente responsable de la hemólisis y la eritropoyesis ineficaz, los dos principales mecanismos fisiopatológicos que causan anemia en pacientes β- talasémicos1,2. El estrés oxidativo (EOx) constituye un factor primordial que influye en el comportamiento y en la gravedad de la anemia de los sujetos con β- talasemia. Últimamente, se ha revelado en sujetos con rasgo β- talasémico un incremento de superóxido dismutasa (SOD) y de malondialdehído (MDA, indicador de peroxidación lipídica) a nivel sistémico3. En este contexto de EOx, se ha demostrado la relevancia fisiopatológica de la eriptosis, un mecanismo de muerte celular específico de los glóbulos rojos, distinto de la hemólisis accidental y de la senescencia celular, en condiciones de anemia4.
De acuerdo con las últimas recomendaciones del Comité de Nomenclatura de Muerte Celular, formuladas en 2018, actualmente, existen dos tipos de muerte celular, a saber, la muerte celular accidental (MAC) y la muerte celular regulada (MCR)5. La MAC es un proceso de muerte celular descontrolado e inevitable que resulta de un estrés severo químico, físico o mecánico, mientras que la MCR puede ser controlada por intervenciones farmacológicas o genéticas. La MCR se divide, además, en formas apoptóticas y no apoptóticas (por ejemplo, ferroptosis, necroptosis, piroptosis, cuproptosis y alkaliptosis), que tienen diferentes características de inducción de señal y modulación molecular, así como implicancias en distintas enfermedades6,7.
La ferroptosis es una forma de MCR no apoptótica, cuyo mecanismo está relacionado con la acumulación de hierro, y es causada por la peroxidación de los lípidos, así como también, por una acumulación excesiva de ERO. El término fue propuesto en 2012 por el laboratorio del Dr. Brent R. Stockwell. Según su estudio original, la ferroptosis es notablemente distinta de otros tipos de MCR, como la apoptosis, la necroptosis y la muerte celular autofágica, morfológica, bioquímica y genéticamente8.
La muerte celular ferroptótica se caracteriza por la acumulación excesiva de Fe2+ libre y la generación de radicales libres altamente reactivos. Un paso crítico e indispensable en la inducción de la ferroptosis es la degradación autofágica de la ferritina, proceso conocido como ferritinofagia9. Esta cascada de eventos, junto a sustratos resultantes de la peroxidación de fosfolípidos que contienen cadenas de ácidos grasos poliinsaturados (PUFA), conduce a una oxidación severa de los fosfolípidos de membrana10,11. Se han identificado múltiples inductores e inhibidores de la ferroptosis que afectan la acumulación de productos de peroxidación lipídica y ERO derivadas del metabolismo del hierro. Paradójicamente, el papel exacto del hierro en la ferroptosis es aún poco claro; sin embargo, su participación está inequívocamente indicada por la fuerte inhibición de la muerte celular asociada con la quelación del hierro o la limitación en la disponibilidad de este metal8. Durante la ferroptosis, se produce el agotamiento del glutatión (GSH) como consecuencia de la inhibición de la captación de cistina o de la inactivación de la selenoproteína glutatión peroxidasa 4 (GPX4), lo que provoca la acumulación de ERO dependientes de hierro y, finalmente, la muerte celular12. Además, la reducción de los niveles de selenio aumenta la susceptibilidad a la ferroptosis debido a la deficiencia de GPX413. Se ha observado que el sistema antiportador de aminoácidos Xc- (compuesto por las proteínas SLC7A11 y SLC3A2) desempeña un rol fundamental en la regulación del estrés oxidativo y la ferroptosis, al ser responsable del intercambio de cistina y glutamato en la membrana celular4. La inhibición de este sistema también puede contribuir a la acumulación de ERO y al desarrollo de la ferroptosis. La función de GPX4 en la reducción de peróxidos de lípidos tóxicos resulta crucial para suprimir la ferroptosis en células normales14.
Se ha demostrado que la ferroptosis está ampliamente involucrada en enfermedades de múltiples sistemas, es decir, enfermedades del sistema nervioso, cardíacas, hepáticas, gastrointestinales, pulmonares, renales y pancreáticas. En cuanto al sistema sanguíneo, se ha descubierto que la ferroptosis juega un papel importante en muchas neoplasias hematológicas, tales como la leucemia, linfoma y mieloma múltiple15.
El gran número de genomas secuenciados en los últimos años condujo a lo que se conoce como era posgenómica. Básicamente, la era posgenómica se caracteriza por el desarrollo de herramientas utilizadas para entender las funciones de un genoma. Una de las herramientas desarrollada fue la proteómica, la cual utiliza la cromatografía líquida acoplada a espectrometría de masas (MS) para la separación de péptidos y posterior identificación de los mismos. Teniendo en cuenta el estrés oxidativo presente en el rasgo β-talasémico (RBT), sumado a un metabolismo del hierro desbalanceado, el propósito del estudio fue determinar si este tipo de MCR, la ferroptosis, podría estar presente en los sujetos portadores de esta anemia hereditaria. Para ello, se identificaron y caracterizaron proteínas de la membrana eritrocitaria implicadas en la ferroptosis en pacientes con RBT mediante MS.
Materiales y Métodos
El estudio incluyó individuos aparentemente sanos (grupo control) y sujetos con RBT (grupo RBT), que fueron detectados en el Instituto de Bioquímica Aplicada de la Universidad Nacional de Tucumán (UNT). El diagnóstico de los portadores de β-talasemia se realizó mediante electroforesis de hemoglobina (Hb) en acetato de celulosa a pH alcalino, y el dosaje de la HbA2, con microcolumna de intercambio iónico (BioSystems, España). Las mutaciones β-talasémicas se estudiaron con PCR tiempo real16. Todos los participantes firmaron una declaración de consentimiento informado aprobado por el Comité de Bioética de la Facultad de Medicina de la UNT.
Para obtener las proteínas de la membrana eritrocitaria, fue necesario extraer la Hb del interior de los mismos, ya que esta proteína se encuentra en gran cantidad en los hematíes y podría interferir en la visualización de las demás proteínas eritrocitarias. De este modo, se obtuvieron glóbulos rojos “fantasmas” y, luego, a partir de las membranas de dichas células, se realizó la cuantificación proteica (Figura 1). Para ello, los glóbulos rojos se separaron por centrifugación a baja velocidad a partir de una muestra de sangre entera anticoagulada con EDTA. Las células aisladas se lavaron con solución fisiológica fría y luego, con un tampón de fosfato sódico (NaH2PO4-Na2HPO4 5 mM más NaCl 150 mM, pH 8). Para extraer la Hb de los glóbulos rojos, la muestra se suspendió en tampón de lisis frío (4°C) (NaH2PO4-Na2HPO4 5 mM, pH 8) durante 5 minutos. El paso de lisis en frío se repitió dos veces más para producir fantasmas blancos con un contenido mínimo de Hb. El pellet obtenido fue finalmente resuspendido en solución fisiológica17.
A partir de las membranas obtenidas con mínimo contenido de Hb, se determinó la concentración de las proteínas de la membrana eritrocitaria. Para ello se determinó la lectura de absorbancia a 280 nm usando un espectrofotómetro UV/Vis para microvolumen DeNovix DS-11+ (Wilmington, USA). Luego, se realizó electroforesis en gel de poliacrilamida SDS (SDS-PAGE). Finalmente, las proteínas de membrana eritrocitaria separadas en el gel se sometieron a análisis por cromatografía líquida con espectrometría de masas (LC-MS/MS) en el Centro de Estudios Químicos y Biológicos en Espectrometría de Masa de la Universidad de Buenos Aires (CEQUIBIEM- CONICET- UBA).
Los espectros obtenidos fueron analizados con el programa Proteome Discoverer V1.4 (Thermo Scientific). Este programa permite identificar los péptidos y asignar un valor de área a cada proteína. Para la identificación de los péptidos, se utilizó la base de datos proteica de Homo sapiens. Una vez obtenidos los valores de área para cada proteína, se normalizaron y calcularon parámetros estadísticos utilizando el programa Perseus V1.5.5.3. Los valores de área fueron expresados como log2.
Se usó la plataforma BlastKOALA para la caracterización funcional de cada proteína18. BlastKOALA es la herramienta que permite relacionar el proteoma de membrana eritrocitaria con diferentes rutas metabólicas asociadas a proteínas relevantes sobrerreguladas. La información obtenida permitió identificar las proteínas involucradas en la patología talasémica y su contexto metabólico.
Las proteínas se consideraron significativamente sobrerreguladas cuando: i) la prueba T de Student mostró un valor de p˂ 0,05; ii) evidenciaron un cambio relativo mayor de 2 (dos) entre las abundancias promedio (fold change> 2). De acuerdo con el programa Perseus, el valor de p se expresó como -log p, donde un valor igual o mayor de 1,3 indicaba una diferencia significativa entre las abundancias. Se calculó también un parámetro denominado T-test Difference RBT-control, que contempla la diferencia entre el promedio de las áreas de cada proteína en las condiciones RBT y control (log2 RBT – log2 control). Así, los parámetros -log p y T-test Difference se utilizaron para construir un gráfico de distribución de proteínas (Volcano Plot). Este gráfico representa la distribución de las proteínas en relación con sus abundancias en ambas condiciones. Para estimar el límite de detección del equipo en cuanto a la abundancia de una proteína, se consideró el percentil noventa y nueve del área de todas las proteínas identificadas por Proteome Discoverer.
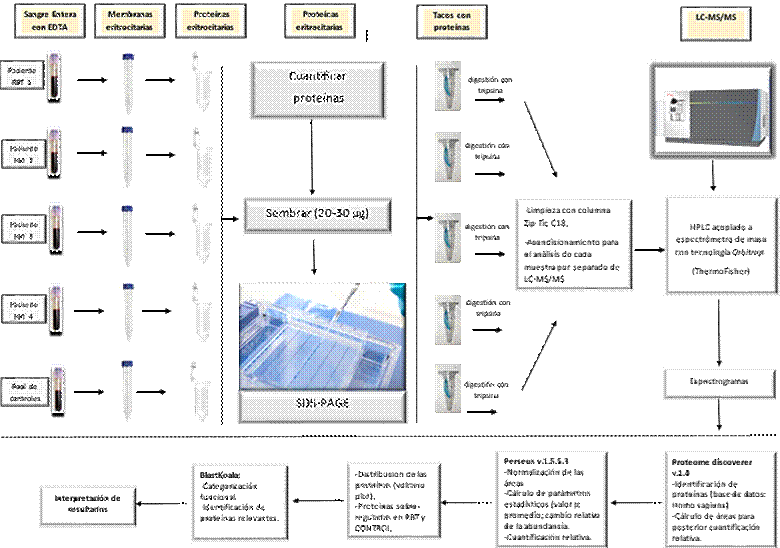
Figura 1.
Esquema de trabajo utilizado para la obtención de péptidos, LC-MS/MS y análisis de datos
Resultados
Se estudiaron 4 (cuatro) sujetos con RBT y 4 (cuatro) individuos aparentemente sanos, todos adultos y de sexo femenino. Dos pacientes β-talasémicas portaban la mutación CD39, mientras que las otras dos exhibieron la mutación IVSI-1.
Del proteoma total detectado (693 proteínas), se identificaron 258 proteínas sobrerreguladas en la condición RBT. La Figura 2 muestra la categorización funcional de las proteínas realizada con el programa BlastKOALA. Se seleccionaron proteínas relevantes relacionadas con el entorno anti / pro-oxidante e inflamatorio; 12 estuvieron sobrerreguladas en el grupo control, y 33, en el grupo RBT (Figura 3). En la Tabla I se muestran las proteínas sobrerreguladas del grupo RBT, involucradas en distintos procesos celulares. En los pacientes con RBT, se detectaron las siguientes proteínas involucradas en la vía ferroptótica: ALOX15 (araquidonato 15-lipooxigenasa) marcadora de peroxidación lipídica, cuya abundancia fue 3 veces mayor que en el grupo control (p< 0,05); PCBP 1 y 2 (Poly(rc)-binding protein 1 y 2), chaperonas del hierro (Fe) que favorecen su depósito, aumentaron significativamente 3,1 y 4,4 veces, respectivamente; P67 y P40, dos subunidades catalíticas de la NADPH oxidasa, estuvieron sobreexpresadas 3,3 y 4,7 veces más en la condición RBT que en los individuos controles (Figura 4).
Asimismo, el estudio proteómico mostró que un marcador de estrés celular inducido por temperatura, compuestos tóxicos o estrés oxidativo, la proteína de shock térmico de 70 kilodalton (HSP 70) y otra proteína implicada en acciones metabólicas y de señalización, la tirosina-proteína quinasa (SYK), aumentaron su abundancia en el grupo RBT. Además, las proteínas involucradas en la protección celular contra el desequilibrio redox, como la glutatión S-transferasa kappa 1 (GSTκ1), la isocitrato deshidrogenasa 1/2 (IDH1/2) y la glucosa-6-fosfato deshidrogenasa (G6PD), mostraron niveles más altos en esta anemia (Figura 4).
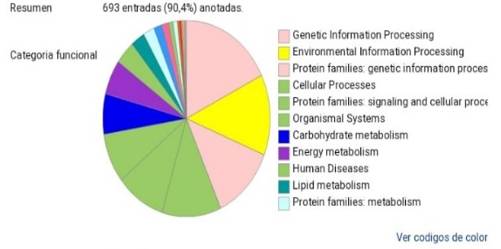
Figura 2.
Categorización funcional mediante BlastKOALA
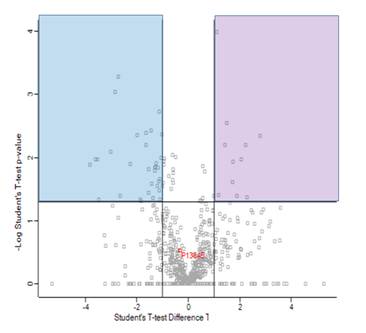
Figura 3.
Volcano plot de las proteínas sobrerreguladas
Color violeta, grupo control; color celeste, grupo rasgo β-talasémico.
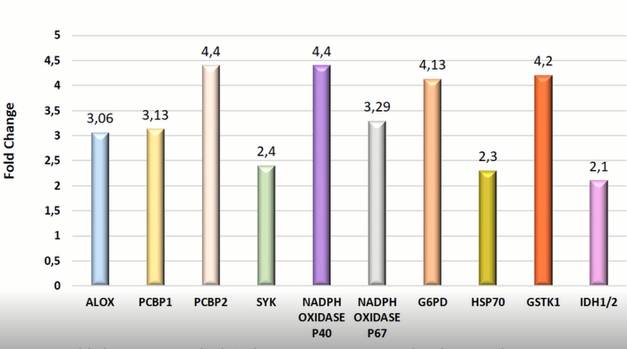
Figura 4.
Abundancia de proteínas sobrerreguladas en el grupo portadores de β-talasemia
ALOX, 15 Araquidonato 15-lipoxigenasa; PCBP1, Poly(rc)-binding protein 1; PCBP2, Poly(rc)-binding protein 2; SYK, Tirosina-proteína quinasa; NADPH, oxidasa subunidad-p40phox; NADPH oxidasa subunidad-p67phox; G6PD, Glucosa-6-fosfato deshidrogenasa; HSP 70, Proteína de shock térmico de 70 kDa; GSTK1, Glutatión s-transferasa kappa 1; IDH1/2, Isocitrato deshidrogenasa 1/2; Fold change, veces del cambio.
Discusión
El fenotipo complejo de las β-talasemias y varias complicaciones relacionadas con el tratamiento subrayan la necesidad de identificar métodos moleculares novedosos para la estratificación de los pacientes y su manejo terapéutico. El uso de metodologías ómicas permite identificar nuevas variantes/secuencias de genes, transcritos, ARN no codificantes, proteínas, metabolitos, etc., involucrados en la patogénesis de la β- talasemia19. En particular, el análisis proteómico proporciona información sobre el papel de las proteínas en los eventos biológicos. A través del análisis de datos multiómicos, Zhou et al. han propuesto que la pérdida de la función del gen de globina β (HBB) en las células progenitoras eritroides humanas conduce a una mayor producción de ERO y de estrés oxidativo, lo que provoca un aumento en la tasa de apoptosis, pero ellos no estudiaron específicamente la ferroptosis20.
Este trabajo presenta el primer conjunto de datos proteómicos que compara la membrana de los glóbulos rojos de los portadores β- talasémicos con la de un grupo control, con respecto al contenido de proteínas implicadas en la ferroptosis. Se reconocieron 5 (cinco) proteínas involucradas en dicha vía: ALOX15, PCBP 1 y 2 y las subunidades de NADPH oxidasa, P40 y P67.
ALOX15 es una enzima que oxida los ácidos grasos poliinsaturados, particularmente los ácidos grasos omega -6 y -3, para generar una serie de metabolitos lipídicos bioactivos. Se expresa constitutivamente en varios tipos de células (reticulocitos, eosinófilos, células dendríticas, macrófagos alveolares, entre otros) y está implicada en una variedad de enfermedades, que incluyen aterosclerosis, hipertensión, diabetes, obesidad y trastornos neurodegenerativos21. Varios autores han demostrado que la peroxidación lipídica catalizada por ALOX15 en las membranas celulares promueve la ferroptosis22,23.
PCBP1 y PCBP2 funcionan como chaperonas de hierro al unirse al metal y facilitar su transferencia a otras proteínas a través de interacciones proteína-proteína mediadas por metales24. PCBP1 desempeña un papel fundamental en la homeostasis del hierro sistémico, ya que ratones knockout (KO) para la PCBP1 hepatocito-específica muestran niveles bajos de ferritina hepática, disfunción mitocondrial y peroxidación lipídica mediada por ERO25. Asimismo, se ha sugerido que las PCBP podrían regular indirectamente los niveles de hierro en los enterocitos mediante la unión de PCBP2 al transportador de metales divalentes 1 (DMT1) y ferroportina (Fpn1), facilitando así la absorción celular de hierro26. Los resultados de varios autores señalan que la regulación negativa de PCBP1/2 se relaciona con la pérdida de la capacidad de los hepatocitos para controlar las reacciones químicas del hierro, lo que sugiere un papel importante en la prevención de la ferroptosis25,27,28. En nuestro estudio, observamos una mayor abundancia de estas chaperonas en pacientes con RBT, lo cual podría indicar un potencial efecto regulador de la ferroptosis.
Es importante destacar que los pacientes incluidos en este estudio mostraron recuentos normales de reticulocitos, lo que indica una respuesta compensatoria adecuada a la anemia, aunque presentaron niveles de ferritina significativamente elevados en comparación con los controles. Es relevante mencionar que ninguno de los pacientes recibió tratamiento con quelantes de hierro, lo que sugiere que los niveles elevados de ferritina podrían ser atribuidos principalmente a la eritropoyesis ineficaz y la sobrecarga de hierro asociada con la β-talasemia. Estos hallazgos, junto con la mayor abundancia de PCBP1 y PCBP2, respaldan el posible papel modulador de estas chaperonas en la ferroptosis en pacientes con RBT.
Las NADPH oxidasas actúan como catalizadores en la formación del radical anión superóxido y la producción de otras ERO, como el peróxido de hidrógeno, que conduce al estrés oxidativo y causa daño a las macromoléculas. La NADPH oxidasa tiene siete isoformas conocidas: NOX1, NOX2, NOX3, NOX4, NOX5, DUOX1 y DUOX2. Estas isoformas se componen de varias subunidades catalíticas centrales: P22phox, P47phox, P67phox, P40phox, DUOX activador 1, DUOX activador, NOXA1 y NOXO129. P67phox es una proteína citosólica no glicosilada que contiene un dominio de activación requerido para la activación de NOX2, mientras que P40phox es una proteína que promueve el ensamblaje de la oxidasa en la membrana30. En el hígado de ratones β- talasémicos Hbbth3/+, la actividad de la NADPH oxidasa se mostró aumentada, aunque no fue a expensas de las isoformas hepáticas más frecuentes, NOX1, NOX2 y NOX431. Por otro lado, Yao et al.32 han demostrado que la inhibición de la NADPH oxidasa atenúa la ferroptosis en un modelo murino de obesidad y diabetes probando la relación de las NADPH oxidasas con este mecanismo de MCR.
El cribado proteómico también permitió reconocer mayor abundancia de proteínas involucradas en el estrés oxidativo y en la inflamación (HSP 70, SYK, GSTκ1, IDH1/2 y G6PD). Asimismo, Kittivorapart et al. describieron el aumento de 19 proteínas en vesículas extracelulares (VEx) presentes en el plasma de individuos con β- talasemia/HbE, entre las cuales se encontraban HSP 70 y enzimas antioxidantes como catalasa, SOD y peroxirredoxina 233. Li et al. también detectaron mayor abundancia de HSP 70 en plasma de pacientes con β- talasemia mayor e intermedia, mientras que Tzounakas et al. reconocieron que proteínas de shock térmico y proteína -quinasas estaban sobrerreguladas tanto en el proteoma de membranas como de VEx eritrocitarias de portadores β- talasémicos34,35. En condiciones normales, HSP 70 transloca al núcleo y protege a GATA1 de la escisión por caspasa-3. En la β- talasemia, el exceso de cadenas de globina α libres secuestra HSP 70 en el citoplasma, impide la expresión normal de GATA1, favorece la apoptosis y provoca una eritropoyesis ineficaz36.
Por otro lado, los perfiles proteómicos de cultivos de células progenitoras eritroides, procedentes de pacientes con β0-talasemia/HbE definieron un estado metabólico oxidativo más activo que el de los controles normales37. El estrés oxidativo en la β- talasemia es consecuencia de la patología molecular caracterizada por el exceso de globina α y por la sobrecarga de hierro, que involucran muchos mecanismos destructivos en el nivel celular y hasta fallas orgánicas en los pacientes que la padecen. La presencia de estrés oxidativo, así como de hierro libre, seguida de una lipoperoxidación lipídica, son eventos previos necesarios para desencadenar la ferroptosis.
Entre las limitaciones del estudio, se puede mencionar el tamaño pequeño de la muestra. Por tal motivo, se necesitaría una investigación más profunda para definir el papel de la ferroptosis en la β- talasemia.
Utilizando proteómica de las membranas celulares de los glóbulos rojos, este trabajo reveló la sobreexpresión de proteínas involucradas en la ferroptosis en portadores de β-talasemia respaldando la idea de que probablemente este tipo de muerte celular no apoptótica desempeñe un papel importante en la fisiopatología de esta anemia hereditaria.
Referencias bibliográficas
1. Mettananda S, Higgs DR. Molecular basis and genetic modifiers of thalassemia.Hematol Oncol Clin North Am 2018; 32(2): 177-91, https://doi.org/10.1016/j.hoc.2017.11.003
2. Oikonomidou PR, Rivella S. What can we learn from ineffective erythropoiesisin thalassemia? Blood Rev 2018; 32(2): 130-43, https://doi.org/10.1016/j.blre.2017.10.001
3. Terán MM, Mónaco ME, Lazarte SS, Haro C, Ledesma Achem E, AsensioNA, Issé BA. Genetic regulation of redox balance in β-thalassemia trait.Hemoglobin 2020; 44(2): 122-7, https://doi.org/10.1080/03630269.2020.1765794
4. Dreischer P, Duszenko M, Stein J, Wieder T. Eryptosis: ProgrammedDeath of Nucleus-Free, Iron-Filled Blood Cells. Cells. 2022;11(3):503,https://doi.org/10.3390/cells11030503
5. Galluzzi L, Vitale I, Aaronson SA, Abrams JM, Adam D, Agostinis P, et al.Molecular mechanisms of cell death: recommendations of the nomenclaturecommittee on cell death 2018. Cell Death Differ 2018; 25: 486-541, https://doi.org/10.1038/s41418-017-0012-4
6. Chen X, Li J, Kang R, Klionsky DJ, Tang D. Ferroptosis: machinery andregulation. Autophagy 2021; 17(9): 2054-81, https://doi.org/10.1080/15548627.2020.1810918
7. Li Y, Du Y, Zhou Y, Chen Q, Luo Z, Ren Y, Chen X, Chen G. Iron and copper:critical executioners of ferroptosis, cuproptosis and other forms of celldeath. Cell Commun Signal. 2023;21(1):327, https://doi.org/10.1186/s12964-023-01267-1
8. Dixon SJ, Lemberg KM, Lamprecht MR, Skouta R, Zaitsev EM, GleasonCE, et al. Ferroptosis: an iron-dependent form of nonapoptoticcell death. Cell 2012; 149(5): 1060-72, https://doi.org/10.1016/j.cell.2012.03.042
9. Latunde-Dada GO. Ferroptosis: Role of lipid peroxidation, iron and ferritinophagy.Biochim Biophys Acta Gen Subj. 2017 ;1861(8):1893-1900, https://doi.org/10.1016/j.bbagen.2017.05.019
10. Galaris D, Barbouti A, Pantopoulos K. Iron homeostasis and oxidativestress: An intimate relationship. Biochim Biophys Acta Mol CellRes 2019; 1866(12): 118535, https://doi.org/10.1016/j.bbamcr.2019.118535
11. Liang D, Minikes AM, Jiang X. Ferroptosis at the intersection of lipidmetabolism and cellular signaling. Mol Cell. 2022;82(12):2215-2227, https://doi.org/10.1016/j.molcel.2022.03.022
12. Yang WS, SriRamaratnam R, Welsch ME, Shimada K, Skouta R, ViswanathanVS, et al. Regulation of ferroptotic cancer cell death by GPX4.Cell 2014; 156: 317-31, https://doi.org/10.1016/j.cell.2013.12.010
13. Xie Y, Kang R, Klionsky DJ, Tang D. GPX4 in cell death, autophagy, anddisease. Autophagy. 2023 ;19(10):2621-2638, https://doi.org/10.1080/15548627.2023.2218764
14. Friedmann Angeli JP, Schneider M, Proneth B, Tyurina YY, Tyurin VA,Hammond VJ, et al. Inactivation of the ferroptosis regulator Gpx4 triggersacute renal failure in mice. Nat Cell Biol 2014; 16(12): 1180-91,https://doi.org/10.1038/ncb3064
15. Zhao Y, Huang Z, Peng H. Molecular mechanisms of ferroptosis and itsroles in hematologic malignancies. Front Oncol. 2021, 27;11: 743006,https://doi.org/10.3389/fonc.2021.743006
16. Lazarte SS, Mónaco ME, Haro AC, Jiménez CL, Ledesma Achem ME,Issé BA. Molecular characterization and phenotyping study of β- thalassemiain Tucumán, Argentina. Hemoglobin 2014; 38 (6): 394-401,https://doi.org/10.3109/03630269.2014.968784
17. Heinrich V, Ritchie K, Mohandas N, Evans E. Elastic thickness compressibiltyof the red cell membrane. Biophys J 2001; 81(3): 1452-63,https://doi.org/10.1016/S0006-3495(01)75800-6
18. Kanehisa M, Sato Y, Morishima K. BlastKOALA and GhostKOALA: KEGGtools for functional characterization of genome and metagenome sequences.J Mol Biol 2016; 428(4): 726-31, https://doi.org/10.1016/j.jmb.2015.11.006
19. Katsantoni E. Omics studies in hemoglobinopathies. Mol Diagn Ther2019; 23(2): 223-34, https://doi.org/10.1007/s40291-019-00386-1
20. Zhou G, Zhang H, Lin A, Wu Z, Li T, Zhang X, et al. Multi-Omics analysisin β-thalassemia using an hbb gene-knockout human erythroidprogenitor cell model. Int J Mol Sci 2022; 23(5): 2807, https://doi.org/10.3390/ijms23052807
21. Singh NK, Rao GN. Emerging role of 12/15-Lipoxygenase (ALOX15)in human pathologies. Prog Lipid Res 2019; 73: 28-45, https://doi.org/10.1016/j.plipres.2018.11.001
22. Shintoku R, Takigawa Y, Yamada K, Kubota C, Yoshimoto Y, Takeuchi T,et al. Lipoxygenase-mediated generation of lipid peroxides enhancesferroptosis induced by erastin and RSL3. Cancer Sci 2017; 108(11):2187-94, https://doi.org/10.1111/cas.13380
23. Cai W, Liu L, Shi X, Liu Y, Wang J, Fang X, et al. Alox15/15-HpETE aggravatesmyocardial ischemia-reperfusion injury by promoting cardiomyocyteferroptosis. Circulation 2023; ;147(19):1444-1460, https://doi.org/10.1161/CIRCULATIONAHA.122.060257
24. Bayır H, Anthonymuthu TS, Tyurina YY, Patel SJ, Amoscato AA, LamadeAM, et al. Achieving life through death: redox biology of lipid peroxidationin ferroptosis. Cell Chem Biol 2020; 27(4): 387-408, https://doi.org/10.1016/j.chembiol.2020.03.014
25. Protchenko O, Baratz E, Jadhav S, Li F, Shakoury-Elizeh M, GavrilovaO, et al. Iron chaperone poly rC binding protein 1 protects mouse liverfrom lipid peroxidation and steatosis. Hepatology 2021, 73: 1176-93,https://doi.org/10.1002/hep.31328
26. Yanatori I, Richardson DR, Imada K, Kishi F. Iron export through thetransporter ferroportin 1 is modulated by the iron chaperone PCBP2.J Biol Chem 2016, 291: 17303-18, https://doi.org/10.1074/jbc.M116.721936
27. Lee J, You JH, Roh JL. Poly(rC)-binding protein 1 represses ferritinophagy-mediated ferroptosis in head and neck cancer. Redox Biol2022; 51: 102276, https://doi.org/10.1016/j.redox.2022.102276
28. Zhang J, Ding N, Xin W, Yang X, Wang F. Quantitative proteomics revealsthat a prognostic signature of the endometrium of the polycysticovary syndrome women based on ferroptosis proteins. FrontEndocrinol (Lausanne) 2022; 13: 871945, https://doi.org/10.3389/fendo.2022.871945
29. Joshi S, Khan SR. NADPH oxidase: a therapeutic target for hyperoxaluria-induced oxidative stress - an update. Future Med Chem 2019;11(23): 2975-8, https://doi.org/10.4155/fmc-2019-0275
30. Chocry M, Leloup L. The NADPH oxidase family and its inhibitors. Antioxid Redox Signal 2020; 33(5): 332-53, https://doi.org/10.1089/ars.2019.7915
31. Bou-Fakhredin R, Dia B, Ghadieh HE, Rivella S, Cappellini MD, Eid AA, TaherAT. CYP450 mediates reactive oxygen species production in a mousemodel of β-thalassemia through an increase in 20-HETE activity. IntJ Mol Sci 2021; 22(3): 1106, https://doi.org/10.3390/ijms22031106
32. Yao W, Liao H, Pang M, Pan L, Guan Y, Huang X, et al. Inhibition of theNADPH oxidase pathway reduces ferroptosis during septic renal injuryin diabetic mice. Oxid Med Cell Longev 2022: 1193734, https://doi.org/10.1155/2022/1193734
33. Kittivorapart J, Crew VK, Wilson MC, Heesom KJ, Siritanaratkul N, ToyeAM. Quantitative proteomics of plasma vesicles identify novel biomarkersfor hemoglobin E/β-thalassemic patients. Blood Adv 2018; 2(2):95-104, https://doi.org/10.1182/bloodadvances.2017011726
34. Li N, An P, Wang J, Zhang T, Qing X, Wu B, et al. Plasma proteome profilingcombined with clinical and genetic features reveals the pathophysiologicalcharacteristics of β-thalassemia. iScience 2022; 25(4):104091, https://doi.org/10.1016/j.isci.2022.104091
35. Tzounakas VL, Anastasiadi AT, Dzieciatkowska M, Karadimas DG, StamoulisK, Papassideri IS, et al. Proteome of stored RBC membrane andvesicles from heterozygous beta thalassemia donors. Int J Mol Sci2021; 22(7): 3369, https://doi.org/10.3390/ijms22073369
36. Arlet JB, Ribeil JA, Guillem F, Negre O, Hazoume A, Marcion G, et al.HSP70 sequestration by free α-globin promotes ineffective erythropoiesisin β-thalassaemia. Nature 2014; 514(7521): 242-6, https://doi.org/10.1038/nature13614
37. Leecharoenkiat A, Wannatung T, Lithanatudom P, Svasti S, FucharoenS, Chokchaichamnankit D, et al. Increased oxidative metabolism isassociated with erythroid precursor expansion in β0-thalassaemia/Hb E disease. Blood Cells Mol Dis 2011; 47(3): 143-57, https://doi.org/10.1016/j.bcmd.2011.06.005
Notas
Notas de autor
magdalena.teran@fbqf.unt.edu.ar
Información adicional
redalyc-journal-id: 651

