Artículos originales
Evaluación de indicadores analíticos en la etapa de posimplementación de un sistema de gestión de calidad en el Área de Química Clínica de un laboratorio de análisis clínicos
Evaluation of analytical indicators after implementation of a quality management system in the clinical chemistry area of a clinical analysis laboratory.
Evaluación de indicadores analíticos en la etapa de posimplementación de un sistema de gestión de calidad en el Área de Química Clínica de un laboratorio de análisis clínicos
Bioquímica y Patología Clínica, vol. 89, núm. 3, pp. 14-18, 2025
Asociación Bioquímica Argentina
Resumen: Introducción: La calidad se ha convertido en los últimos años en la meta fundamental de los laboratorios de análisis clínicos. El principal objetivo es garantizar la seguridad del paciente, a expensas de sistemas rigurosamente controlados, tanto en la etapa analítica como en el resto de los procesos. Objetivo: Evaluar la evolución de indicadores de calidad (IC) analíticos, en las etapas de pre y posimplementación de un sistema de gestión de calidad (SGC), en el área de química clínica de un laboratorio de análisis clínico. Materiales y métodos: Se evaluó el desempeño de 28 analitos y se utilizaron tres IC: Sigma (IS), Incertidumbre de Medida (IU) y Evaluación Externa de la Calidad (IEEC). Se realizaron mediciones mensuales de los analitos y se analizaron los resultados en los períodos de pre y posimplementación del sistema de gestión de calidad. Se utilizó la plataforma analítica Cobas 8000 de Roche Diagnostic, módulo c502. Resultados: Comparando las etapas de pre y posimplementación del sistema de gestión de calidad, los resultados obtenidos arrojaron diferencias estadísticamente significativas, y, para todos los indicadores evaluados, se observó una mejora en el desempeño. Conclusión: El uso de indicadores de calidad en la etapa analítica fue efectivo para monitorear correctamente el desempeño de los analitos evaluados permitiendo documentar en forma objetiva la mejora tanto del control de calidad interno como del externo. Implementar un sistema de gestión de calidad posibilitó mejorar el desempeño analítico.
Palabras clave: gestión de calidad, indicadores de calidad, calidad analítica.
Abstract: Introduction: In recent years, quality has become the fundamental goal of clinical analysis laboratories. The main objective is to guarantee patient safety, at the expense of rigorously controlled systems, both at the analytical stage and in the remaining processes. Objective: To evaluate the evolution of analytical Quality Indicators (QIs), before and after implementation of a Quality Management System (QMS), in the clinical chemistry area of a clinical analysis laboratory. Materials and methods: The performance of 28 analytes was evaluated and three QIs were used: Sigma Indicator (SI), Measurement Uncertainty Indicator (MUI) and External Quality Evaluation Indicator (EQEI). The analytes were monthly measured and the results were analyzed in the pre- and post-implementation periods of the QMS. The Roche Diagnostic cobas 8000 analytical platform, module c502, was used. Results: When comparing the pre- and post-implementation stages of the QMS, the results obtained showed statistically significant differences for all the indicators evaluated, and an improvement in the performance of the indicator was observed. Conclusion: The use of QIs at the analytical stage was effective to correctly monitor the performance of the analytes evaluated, allowing to objectively document the improvement of both internal and external quality control. Implementing a QMS allowed improving the analytical performance.
Keywords: quality management, quality indicators, analytical quality.
Introducción
El concepto de calidad ha evolucionado a lo largo de los años en el laboratorio clínico. Antiguamente, se creía que el solo análisis de muestras control, cuyos resultados estuvieran dentro del rango establecido por el fabricante, garantizaba resultados correctos desde el punto de vista analítico.
En la actualidad, se conoce que la corrida de controles de calidad internos es solo el primer paso para la gestión de calidad analítica, y es necesario contar con procedimientos detallados de todos los procesos involucrados.
Uno de los principales organismos encargado de desarrollar normas técnicas internacionales de calidad es la International Organization for Standardization (ISO), y su principal objetivo es unificar normas que permitan la mejor coordinación internacional entre las instituciones1. Con el propósito de evaluar la calidad y competencia técnica de los laboratorios clínicos, el Comité Técnico ISO/TC 212 (Clinical Laboratory Testing and In Vitro Diagnostic Systems) desarrolló la Norma ISO 151892, teniendo como referencia la Norma ISO 9001 y la ISO/IEC 17025. La mencionada norma está dividida en dos partes: la de gestión pertinente a los requerimientos para la certificación del sistema de gestión de calidad (SGC) y la parte técnica, que detalla los requisitos para el personal, instalaciones, equipos, procedimientos, informes y garantía de calidad.
La meta principal de trabajar bajo estándares de calidad bien definidos es obtener un resultado confiable, oportuno y trazable que contribuya a un diagnóstico efectivo para la salud del paciente3.
En la actualidad, el laboratorio clínico provee información crítica para la pesquisa, monitoreo, prevención y tratamiento de distintas patologías. En los últimos años, se observó un crecimiento importante en la demanda de ensayos analíticos, en gran parte, por el desarrollo de nuevas determinaciones, la mayor accesibilidad a las mismas y la disminución en los tiempos de espera de los resultados. Como consecuencia, los laboratorios deberían desarrollar un SGC con el fin de poder garantizar la calidad de los procesos y servicios que brindan las instituciones4.
Antes de implementar un SGC se deben conocer las necesidades de los pacientes y usuarios, evaluar cómo cumplirlas y, con base en esto, planificar los procesos involucrados, desarrollar métodos para cuantificar su eficacia y evaluar en forma objetiva la mejora continua5.
La implementación de indicadores de calidad (IC) orientados a monitorear determinados procesos permite cuantificar la calidad con la que se trabaja6, a la vez que establecer límites y aplicar acciones correctivas cuando estos se superen. Numerosas instituciones han desarrollado IC para evaluar el desempeño de las distintas etapas del proceso de trabajo en el laboratorio clínico, entre ellas, se destacan la Internacional Federation of Clinical Chemistry (IFCC) y el Laboratory Medicine Working Group on Laboratory Errors and Patient Safety, que, con base el consenso “Harmonization of quality indicators in laboratory medicine. A preliminary consensus”7, establecieron una puntuación de prioridad para resaltar el valor de cada IC de manera individual, a fin de evaluar no solo la calidad del servicio y los posibles efectos sobre la seguridad del paciente, sino también la viabilidad de la recopilación de datos8.
Los límites de los distintos IC son establecidos sobre la base de resultados obtenidos de numerosos laboratorios que participan del programa diseñado por la IFCC y pueden ser extraídos de su página web9. Se considera el percentil 25 como performance de alta calidad para un indicador, el percentil 50, de calidad media y el percentil 75, como de baja calidad.10
El objetivo del estudio fue evaluar la evolución de indicadores de calidad analíticos en el área de química clínica de un laboratorio de análisis clínico en las etapas de pre y posimplementación de un sistema de gestión de calidad con base en la Norma ISO 15189:201411.
Materiales y métodos
Se realizó un estudio observacional, retrospectivo y longitudinal. Se evaluaron durante tres años los resultados obtenidos para los IC que se citan a continuación. Para realizar la comparación se los dividió en dos etapas, la de preinplementación (PREI) y la de posimplementación (POSI) de un SGC en el Laboratorio de Análisis Clínicos Dres. de Elias y Kiener SRL de la Ciudad de Córdoba (Laboratorio Central del Sanatorio Allende, sede Cerro).
Indicadores de calidad
Con base en lo descrito por la IFCC y en trabajos desarrollados por profesionales en nuestra región12, se utilizaron tres IC para evaluar el desempeño de la etapa analítica: Sigma (IS), Incertidumbre de Medida (IU) y Evaluación Externa de la Calidad (IEEC). El fin de los mencionados indicadores es identificar analitos con bajo desempeño en el control de calidad interno y la evaluación externa de la calidad. Los indicadores fueron registrados, en una primera instancia, de manera manual en una planilla de cálculo de Microsoft Excel ®. Se midieron los IC de manera mensual durante tres años.
Indicador Sigma (IS)
La fórmula empleada para calcular dicho indicador fue: Sigma = (número de analitos con sigma inaceptable/total de analitos)*100. Para el cálculo de Sigma se utilizó la siguiente fórmula: Sigma = %error total permitido-% desvío / %coeficiente de variación (CV) 13. Los datos fueron extraídos del programa interlaboratorio TIQCon de Roche Diagnostics14, que provee de manera mensual datos del desempeño de cada analito.
-
INACEPTABLE: Sigma <2
MARGINAL: Sigma= 2-3
ACEPTABLE: Sigma= 3,1-4
BUENO: Sigma= 4,1-5,9
Seis SIGMA: sigma ≥6
Indicador Incertidumbre de medida (IU)
La fórmula para el cálculo fue: IU= (número de analitos con valor crítico de incertidumbre/total de analitos)*100. Al igual que el IS, IU también se obtiene del programa TIQCon, de manera mensual. Esta herramienta nos provee los valores de incertidumbre calculada con factor dos (U(k=2)) e incertidumbre calculada en porcentaje (U(k=2)%), ambas expresadas en términos de percentil, sobre la base de los datos obtenidos del grupo par. Se consideran óptimos valores obtenidos por debajo del percentil 50 (U50), buenos valores inferiores al percentil 90 (U90) y críticos por encima del percentil 90.
Indicador Evaluación Externa de la Calidad (IEEC)
La fórmula para el cálculo fue: IEEC = (número de analitos rechazados por muestra/total de analitos)*100. Para el seguimiento de IEEC, se utilizaron los reportes obtenidos del Programa Internacional de Evaluación Externa de Calidad para Laboratorios de Análisis Clínicos Argentinos y Extranjeros (ProgBA)15, que consta de veinticuatro muestras por ronda, de presentación liofilizada, a ensayar en períodos de quince días. Los resultados obtenidos para cada muestra se clasifican según analizador, método, marca de reactivo y en general.
Resultados
Los valores medidos para los distintos indicadores PREI y POSI, expresados en términos de porcentaje, se compararon utilizando el test no paramétrico de Mann-Whitney para variables independientes.
El IS fue determinado para 28 analitos de química clínica, en dos niveles de concentración de control PreciControl ClinChem Multi 1 y 2 (PCC1 y PCC2); los resultados obtenidos no se incluyen en este trabajo. Sin embargo, están disponibles para ser solicitados a los autores. Se comparó el porcentaje de analitos con IS inaceptable PREI y POSI, y se observó una diferencia estadísticamente significativa (p= 0,023) (Figura 1). Como se puede observar en la Figura 2, durante la fase de PREI el número de analitos con Sigma inaceptable era evidentemente más elevado que en la de POSI. El 79 % de los analitos mejoró su sigma POSI con respecto a PREI para PCC1 y el 71%, para PCC2.
De la comparación realizada para el indicador IU se obtuvo una diferencia estadísticamente significativa (p=0,0031), como se observa en la Figura 3. En la Figura 4, se detalla el comportamiento del IU en las distintas etapas, en las que se observó mayor porcentaje de analitos con valores críticos de incertidumbre durante la PREI.
Para el cálculo del indicador IECC, se tomaron tres rondas de ProgBA para abarcar las dos etapas (PREI y POSI), y se constataron diferencias estadísticamente significativas entre las mismas (p=0,0163) (Figura 5).
En la Figura 6, se ven reflejados los porcentajes de analitos rechazados por muestra de evaluación externa de la calidad (IEEC) en las etapas de pre y posimplementación del SGC.
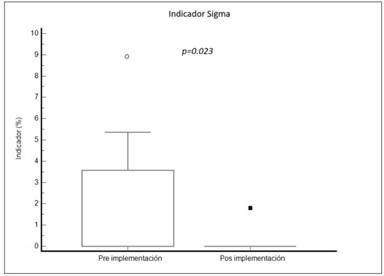
Figura 1
Comparación en porcentaje de sigmas inaceptables (IS) en las etapas de pre y pos- implementación del sistema de gestión de calidad
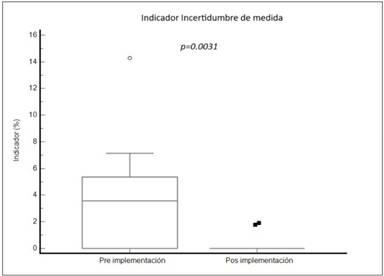
Figura 3
Comparación en porcentaje de analitos con valor crítico de incertidumbre (IU) en las etapas pre y posimplementación del sistema de gestión de calidad
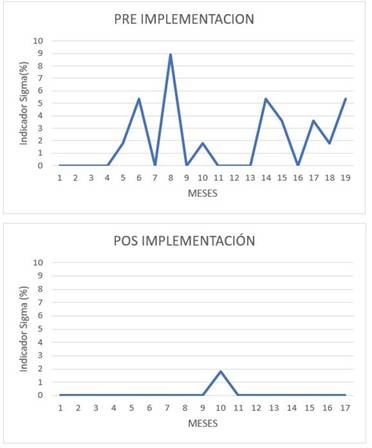
Figura 2
Comparación en porcentaje de analitos con sigma inaceptable (IS) durante los distintos meses de pre y posimplementación del sistema de gestión de calidad
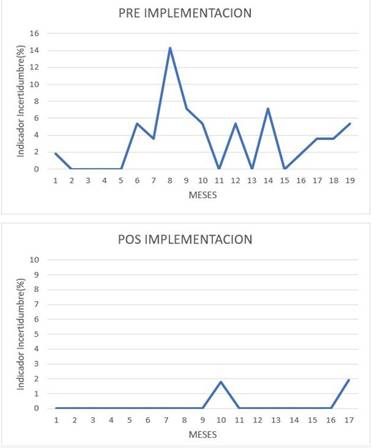
Figura 4
Comparación en porcentaje de analitos con valor crítico de incertidumbre (IU) durante los distintos meses de pre y posimplementación del sistema de gestión de calidad
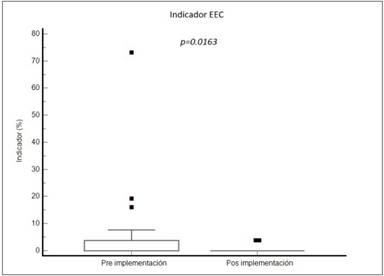
Figura 5
Porcentaje de analitos rechazados por ronda de evaluación externa de la calidad (IEEC) en las etapas de pre y posimplementación del sistema de gestión de calidad
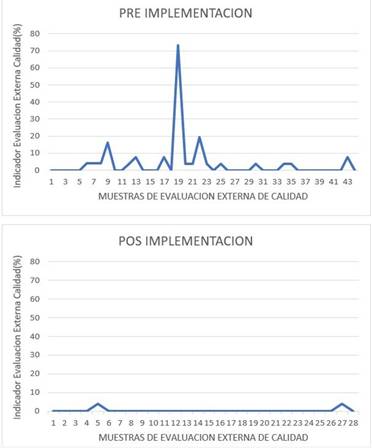
Figura 6
Comparación en porcentaje de analitos rechazados por muestra de evaluación externa de la calidad (IEEC) en las etapas de pre y posimplementación del sistema de gestión de calidad
Discusión
El proceso de implementación de un SGC ha implicado el desarrollo de una serie de procedimientos a ejecutar, elaborados con base en lo establecido en los distintos puntos de la Norma ISO 15189:2014, para estandarizar todos los procesos.
En la etapa analítica del área de química clínica, se implementó un programa de mantenimiento de equipos, con la ejecución en tiempo y forma de todos los mantenimientos preventivos, según la recomendación del fabricante de la plataforma analítica; este procedimiento fue acompañado de un plan de capacitación del personal en todas las etapas que comprende el proceso analítico. Se llevó a cabo la verificación de métodos partiendo del establecimiento de requisitos de calidad, contemplando las distintas fuentes disponibles (Ej.: EFLM, RIQAS, CLIA)16, seguida de la verificación de precisión y veracidad según EP15A317, verificación de la linealidad según EP6A18 y verificación de valores de referencia según EP28A3C.19
Se llevó a cabo la planificación de control de calidad interno incluyendo la verificación de cada nuevo lote control; se realizó la evaluación mensual del desempeño analítico de cada analito implementando reglas de control, teniendo en cuenta el tamaño de corrida analítica; se empleó el QC frecuency calculator de Westgard.20 Se capacitó al personal para el manejo del programa interlaboratorio TIQCon.
Se estandarizaron los procesos de reconstitución de material control y calibradores empleando pipetas de doble aforo calibradas. Se implementó la verificación de cada nuevo lote de reactivo21; la verificación periódica de la comparabilidad de resultados de diferentes plataformas analíticas del mismo laboratorio22; la verificación de la comparabilidad de resultados ante el ingreso de nuevos consumibles al laboratorio; el análisis de estabilidad de cada analito y la participación en programas de evaluación externa de la calidad.
Sumado a todos los puntos antes expuestos, se capacitó a todo el personal implicado, siendo este uno de los aspectos fundamentales para asegurar que el trabajo se realice según lo citado en los distintos procedimientos e instructivos que se desarrollaron.
Con base en lo publicado en distintos trabajos, como el de Min Duan et al23 sobre el valor de los IC a la hora de evaluar y monitorear las fases intraanalítica y extraanalítica de la calidad, se determinó la utilización de IC como herramienta para evaluar el impacto de la implementación del SGC en términos de desempeño analítico, y se constató una mejora estadísticamente significativa en los resultados obtenidos PREI y POSI para todos los IC evaluados.
Ana Belén Pacheco et al12 establecieron que la implementación de un SGC bajo los requisitos de normas internacionales mejoró el conocimiento y funcionamiento de los procesos del laboratorio clínico; resultados similares se obtuvieron en el presente estudio luego de implementar un SGC, y se observó mejora en el desempeño de los indicadores IS, IU e IEEC. El monitoreo de los mencionados IC es una medida objetiva del desempeño analítico de los procedimientos de medida, lo cual facilita la implementación de acciones correctivas y preventivas.
El desarrollo de un SGC ayuda a garantizar el cumplimiento de normativas y regulaciones al establecer protocolos y prácticas que se ajustan a los requisitos establecidos por organismos gubernamentales y de acreditación.
Conclusión
La implementación de un sistema de gestión de calidad mostró un impacto positivo en el desempeño del laboratorio, evidenciado en la mejora de los indicadores analíticos (IS, IU e IEEC). La utilización de indicadores de calidad permitió monitorear procesos críticos dentro de la etapa analítica asegurando que los procesos cumplan con las normativas y estándares establecidos por la Norma ISO 15189:2014.
La implementación de un sistema de gestión de calidad mostró un impacto positivo en el desempeño del laboratorio, evidenciado en la mejora de los indicadores analíticos (IS, IU e IEEC). La utilización de indicadores de calidad permitió monitorear procesos críticos dentro de la etapa analítica asegurando que los procesos cumplan con las normativas y estándares establecidos por la Norma ISO 15189:2014.
Agradecimientos
Al Laboratorio de Análisis Dres. de Elías y Kiener SRL por brindarme las herramientas para la confección del presente trabajo, en especial, a la DT Bioq. Gisel Kiener por su apoyo; a mi tutor de especialidad, Bioq. Esp. Rafael de Elías; a la Bioq. Silvia Barzon y a todos mis compañeros del laboratorio del área de química clínica, en especial, a Cynthia y Rocío.
Referencias bibliográficas
1. Soto E, Isabel J. Conocimiento de NTP ISO 15189 y relación con la implementación de estándares del laboratorio clínico por tecnólogos médicos, Lima 2021. Universidad César Vallejo; 2022.
2. Suscriptor. ISO 15189: Sistema de Gestión de la Calidad en Laboratorios Clínicos [Internet]. Software ISO. ISOTools; 2014 [citado 7 de febrero 2024]. Disponible en: https://www.isotools.us/2016/02/29/iso-15189-sistema-gestion-calidad-en-laboratorios-clinicos/
3. Carboni-Huerta R, Sáenz-Flor K. Acreditación ISO 15189 en América Latina: Percepción en laboratorios de la región. Rev Mex Patol Clin Med Lab. 2019;66(3):143-153.
Fraiz FJ. Organización funcional de los laboratorios de análisis clínicos. Rev Diagn Biol [Internet]. 2003 Mar [citado 2024 Jul 04] ; 52(1): 40-5. Disponible en: https://scielo.isciii.es/scielo.php?script=sci_arttext&pid=S0034-79732003000100006
Cantero, F. (2015). Estudio de indicadores de calidad en pruebas de laboratorio realizadas en el lugar de asistencia al paciente [Tesis doctoral]. Universidad de Málaga. Disponible en: https://riuma.uma.es/xmlui/bitstream/handle/10630/12487/TD_CANTERO_SANCHEZ_Miguel_An gel.pdf?sequence=1
6. Viteri C, Ramos M, Galarraga E. Indicadores de control de calidad en laboratorios clínicos del C antón Ambato, Ecuador, 2021. Revista GICOS. 2023;8(1):40–99, https://portal.amelica.org/ameli/journal/351/3514065004/html/
7. Plebani M, Astion ML, Barth JH, Chen W, de Oliveira Galoro CA, Escuer MI, et al. Harmonization of quality indicators in laboratory medicine. A preliminary consensus. Clinical Chemistry and Laboratory Medicine (CCLM). 2014;52(7):951-8, https://doi.org/10.1515/cclm-2014-0142
8. International Federation of Clinical Chemistry and Laboratory Medicine Working Group “Laboratory Errors and Patient Safety”. Model of quality indicators. Milano, Italia: IFCC; 2017.
9. Sepetiene R. Quality indicators in laboratory medicine. Am J Biomed Sci Res [Internet]. 2021 [citado 2024 Feb 7];14(6):571–2. Disponible en: https://ifcc.org/ifcc-education-division/working-groupsspecial-projects/wg-leps/quality-indicators-project/. DOI: 10.34297/AJBSR.2021.14.002059
10. Sciacovelli L, Padoan A, Aita A, Basso D, Plebani M. Quality indicators in laboratory medicine: state-of-the-art, quality specifications and future strategies. Clin Chem Lab Med 2023;61(4):688–95, http://dx.doi.org/10.1515/cclm-2022-1143
11. Organización Internacional de Normalización. Laboratorios Clínicos. Requisitos para la calidad y la competencia. NM ISO 15189:2014. Argentina
12. Pacheco AB, Silvia Zamory E, Collino CJG. Impacto de la implementación de un sistema documental en el aseguramiento de la calidad en un laboratorio de análisis clínicos de un hospital público. 2019;53(4): 511-24, https://www.redalyc.org/articulo.oa?id=53562809013
13. Carchio SM, Cappella AC, Goedelmann C, Pandolfo M, Bustos D. Aplicación de Seis Sigma en el Laboratorio Clínico. Acta Bioquím Clín Latinoa [Internet]. 2019 Dic [citado 2024 Jul 09]; 53(4):525-537. Disponible en: https://www.redalyc.org/journal/535/53562809014/html/
14. TIQConTM - Quality Desktop [Internet]. Tiqcon.com. [citado 2024 Feb 7]. Disponible en: https://roche.tiqcon.com/QD/Index/desktop
15. Control de Calidad Externo - Acceso de laboratorios [Internet]. [citado 2024 Feb 7]. Disponible en: http://200.69.143.220/cce/cgi/ CCE.cgi?AccionServidor =AccionAccesoLaboratorios
16. Westgard S. Consolidated comparison of chemistry performance specifications [Internet]. Westgard.com. [citado 2024 Feb 7]. Disponible en: https://www.westgard.com/ clia-a-quality/ quality-requirements/consolidated-comparison-of-chemistry-performance-specifications.html
17. Clinical and Laboratory Standard Institute (CLSI). User Verification of Precision and Estimation of Bias; Approved Guideline-Third Edition. EP15-A3. Wayne, PA; 2014.
18. Clinical and Laboratory Standard Institute (CLSI). Evaluation of Linearity of Quantitative Measurement Procedures. 2nd ed EP06A. 2020.
19. Clinical and Laboratory Standard Institute (CLSI). Defining, Establishing, and Verifying Reference Intervals in the Clinical Laboratory. EP28A3C 2010.
20. QC Frequency Calculator [Internet]. Westgard.com. [citado el 9 de julio de 2024]. Disponible en: https://tools.westgard.com/frequency_calculator.shtml
21. Clinical and Laboratory Standard Institute (CLSI). User Evaluation of Between-Reagent Lot Variation; Approved Guideline. CLSI document. Wayne, PA: Clinical and Laboratory Standards Institute; EP26-A 2013.
22. Clinical and Laboratory Standard Institute (CLSI). Measurement Procedure Comparison and Bias Estimation Using Patient Samples; Approved Guideline-Third Edition. EP09-A3. Wayne, PA: Clinical and Laboratory Standards Institute; 2013.
23. Duan M, Ma X, Fan J, Guo Y, Wang W, Zhao H, et al. National surveys on 15 quality indicators for the total testing process in clinical laboratories of China from 2015 to 2017. Clin Chem Lab Med. 2018;57(2):195–203, http://dx.doi.org/10.1515/cclm-2018-0416
Notas
Notas de autor
lcolazo@sanatorioallende.com
Información adicional
redalyc-journal-id: 651

