Artículos originales
Anticuerpos heterófilos como interferentes en la determinación de autoanticuerpos por inmunoflurescencia indirecta.
Heterophilic antibodies as interfering agents in the determination of autoantibodies by indirect immunofluorescence
Anticuerpos heterófilos como interferentes en la determinación de autoanticuerpos por inmunoflurescencia indirecta.
Bioquímica y Patología Clínica, vol. 87, núm. 2, pp. 21-25, 2023
Asociación Bioquímica Argentina
Resumen: Los anticuerpos heterófilos (AH) están dirigidos contra antígenos de otra especie. Estos anticuerpos pueden mimetizar autoanticuerpos específicos y llevar a errores diagnósticos en el estudio por inmunofluorescencia indirecta (IFI). Objetivos: Destacar la importancia de reconocer las imágenes características de los AH y analizar la incidencia de los mismos en muestras de pacientes que asisten a laboratorios hospitalarios. Materiales y métodos: Se realizó un estudio observacional, longitudinal, prospectivo y analítico donde se evaluó la presencia de AH en suero, en 2 cohortes de pacientes que ingresaron de manera consecutiva para el estudio de anticuerpos específicos en dos hospitales de la Ciudad de Buenos Aires (n = 661). Se utilizó la técnica de IFI sobre cortes de hígado, riñón y estómago de rata. Resultados: La incidencia de los AE fue mayor que la de los AH (19,2 % vs 10,1 %), APCA, ASMA, AMA (6,8/6,2/5,7 %, respectivamente), y LKM (0,4 %) fue el de menor incidencia. No se encontró concomitancia entre AH y AE en las dos cohortes estudiadas. Se observaron los siguientes patrones de AE: ribete en cepillo (RC): 7,1 %, células parietales (CP): 5,6 % y músculo liso (ML): 3,2 %, células de Kupffer (CK): 0,4 %. Se describe la presencia de más de un patrón de AE por paciente. Conclusiones: Si bien la frecuencia de AE es mayor que la de AH, estos últimos estuvieron presentes en el 10,1 % de los pacientes incluso hasta con 3 patrones característicos concomitantemente. Es de suma importancia que el observador esté entrenado para distinguirlos, ya que podrían mimetizar los AE y llevar a una interpretación errónea de los resultados.
Palabras clave: autoanticuerpos, heterófilos, inmunofluorescencia indirecta.
Abstract: Heterophilic antibodies (HA) are directed against antigens from another species. These antibodies can mimic specific autoantibodies, leading to diagnostic errors in the study by indirect immunofluorescence (IIF). Objectives: To highlight the importance of recognizing the characteristic images of HA and to analyze their incidence in samples from patients attending hospital laboratories. Materials and methods: An observational, longitudinal, prospective and analytical study was carried out. The presence of HA in serum was evaluated in two cohorts of patients, who had been admitted consecutively for the study of specific antibodies in two hospitals in the City of Buenos Aires (n=661). The IIF technique was used on rat liver, kidney and stomach sections. Results: The incidence of specific antibodies was higher than that of HA (19.2 % vs 10.1 %), APCA (6.8), ASMA, (6.2) AMA (5.7 %) and LKM (0.4 %). No concomitance between HA and specific antibodies was found in the two cohorts studied. Among the characteristic patterns of HA, the coloration of the brush border was 7.1 %, parietal cells 5.6 % and smooth muscle 3.2 %, and Kupffer cells 0.4 %. Conclusions: Although the frequency of specific antibodies was higher than that of HA, the latter were present in 10.1 % of the patients and with up to three concomitant characteristic patterns. Thus, it is of utmost importance that the observer is trained to identify HA, since they could mimic specific antibodiesand this could lead to misinterpretation of the results.
Keywords: Autoantibodies, Heterophile, Indirect Immunofluorescence.
Introducción
El término anticuerpos heterófilos (AH) (del griego, hetero: diferente y filo: afinidad) es usado para describir anticuerpos humanos dirigidos contra antígenos de origen animal más que contra antígenos humanos. Estos anticuerpos interfieren en muchas determinaciones del laboratorio. The Taber´s Medical Dictionary los define como anticuerpos en respuesta a cualquier antígeno distinto del específico.1 Por lo tanto, una definición un poco más completa sería que los AH reaccionan con antígenos xenoespecíficos y aloespecíficos más que con antígenos de tejidos específicos.2
En la práctica clínica diaria, durante la investigación de autoanticuerpos, tales como los antimitocondriales (AMA), antimúsculo liso (ASMA), anti-células parietales (APCA) y antimicrosomales de hígado y riñón (anti-LKM) (Foto: a, c, e y g) por la técnica de inmunofluorescencia indirecta (IFI), utilizando como sustrato cortes criostáticos de hígado, riñón y estómago de rata, la presencia de AH pueden guiarnos a una interpretación errónea del resultado. Resultados falsos positivos pueden ser encontrados cuando los AH reaccionan con células parietales del estómago (CP) o ribete en cepillo (RC) de los túbulos renales, contra estructuras intersticiales presentes en el músculo liso (ML) del estómago de la rata o contra células de Kupffer (CK) en el hígado (Foto: b, d, f y h) mimetizando los patrones específicos antes mencionados.2,3,4,5
El objetivo del presente trabajo es destacar la importancia de reconocer los patrones inespecíficos de los sueros con AH para evitar interpretaciones erróneas en la investigación de autoanticuerpos por inmunofluorescencia y asimismo, reportar la incidencia de los AH, en comparación con la presencia de anticuerpos específicos (AE) en los sueros recibidos para el estudio de autoanticuerpos mencionados anteriormente.
Materiales y métodos
Se realizó un estudio observacional, longitudinal, prospectivo y analítico en dos hospitales de la Ciudad Autónoma de Buenos Aires, de manera simultánea. Se analizaron 661 muestras consecutivas, recibidas 338 en el Hospital Italiano de Buenos Aires (HIBA) y 323 en el Hospital Carlos G. Durand (HD) para el estudio de AMA, ASMA, anti-LKM, y se consignó , además, la presencia de AH.
La técnica de IFI se realizó de manera convencional, utilizando como sustrato cortes criostáticos de hígado, riñón y estómago de rata (BioSystems™). Como segundo anticuerpo, marcado con isotiocianato de fluoresceína, se usó un anticuerpo anti-IgG humana de cabra (Biocientífica®). Se incubaron sobre el sustrato, en cámara húmeda, diluciones del suero (1:40) en buffer fosfato (PBS) durante 30 minutos. Posteriormente, se realizaron un lavado rápido y dos lavados con PBS de 5 minutos. Seguidamente, el suero se incubó 30 minutos con anti-IgG humana, marcada con isotiocianato de fluoresceína, en dilución apropiada; nuevamente se realizaron un lavado rápido y 2 lavados de 5 minutos con PBS. Las improntas se cubrieron con líquido de montaje y un cubreobjeto y fueron observadas en el microscopio con aumento 400x por dos operadores independientes.
Para analizar las diferencias proporcionales en los resultados encontrados en los dos centros, se utilizó la prueba de Chi2 y se consideraron significativos los resultados cuando se obtuvo una p < 0,05.
Resultados
Se analizaron 661 muestras totales: 338, en HIBA y 323, en HD. El 19,2 % (HIBA 24 % - HD 13,2 %) de las muestras estudiadas mostraron un patrón específico positivo (Tabla I). Los patrones más frecuentemente encontrados fueron: APCA (6,8 %), ASMA (6,2 %) y AMA (5,7 %) (Figura1). El anticuerpo anti-LKM fue encontrado solamente en un 0,4 % (HIBA 0,6 % - HD 0,3 %) (Figura 1) (Tabla I). El total de AH hallados fue de 10,1 % (8 % HIBA y 12,5 % HD). No se identificaron anticuerpos heterófilos concomitantemente con la presencia de anticuerpos específicos (Figura 2). El patrón de AH más comúnmente hallado en el total de las muestras estudiadas fue el RC (7,1 %) seguido por CP (5,6 %), ML (3,2 %) y, por último, CK (0,4 %) (Tabla II). El RC se encuentra en el 70,1 % de las muestras que presentan positividad para AH, seguido por CP (55,2 %), ML (31,3 %), y, por último, CK (4,5 %) (Figura 3). Cabe destacar que el patrón que tiñe las CK se presentó en el 0,4 % de las muestras y siempre estaba acompañado por tinción de las CP del estómago y RC de los túbulos. En el 68,4 % de los casos los AH del tipo CP estaban acompañados por la tinción en RC. En este mismo sentido, cuando la tinción de ML estaba presente, en el 100 % de los casos, estaba acompañada por RC y en el 72 % de las veces, además, se observaba tinción en CP.
| Ac Esp | APCA | ASMA | AMA | LKM | Total Esp | n |
| HIBA | 30 (8,8 %) | 29 (8,6 %) | 22 (6,5 %) | 2 (0,6 %) | 83 (24 %) | 338 |
| HD | 15 (4,7 %) | 12 (3,7 %) | 16 (5 %) | 1 (0,3 %) | 44 (13,7 %) | 321 |
| Total | 45 (6,8 %) | 41 (6,2 %) | 38 (5,7 %) | 3 (0,4 %) | 127 (19,2 %) | 661 |
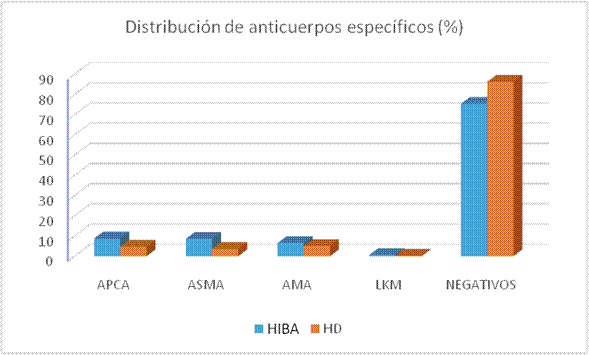
Figura 1.
Distribución porcentual de anticuerpos específicos
APCA, anticuerpos anti células parietales; ASMA, anticuerpos anti-músculo liso; AMA, anticuerpos anti-mitocondriales; LKM, anticuerpos antimicrosomales del hígado y el riñón; HIBA, Hospital Italiano; HD, Hospital Durand.
| AH | CP | RC | ML | CK | AH (pos) | AH totales | n |
| HIBA | 18 (5,3 %) | 17 (5 %) | 6 (1,8 %) | 2 (0,6 %) | 27 (8,0 %) | 43 (12,7 %) | 338 |
| HD | 19 (5,9 %) | 30 (9,3 %) | 15 (4,7 %) | 1 (0,3 %) | 40 (12,5 %) | 65 (2,2 %) | 321 |
| Total | 37 (5,6 %) | 47(7,1 %) | 21 (3,2 %) | 3 (0,4 %) | 67 (10,1 %) | 108 (16,3 %) | 661 |
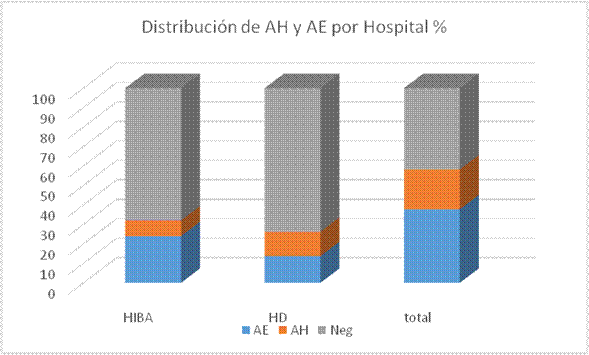
Figura 2.
Distribución porcentual de anticuerpos heterófilos
AE, anticuerpos específicos; AH, anticuerpos heterófilos; HIBA, Hospital Italiano; HD, Hospital Durand; Total, corresponde al porcentaje total de muestras positivas y negativas totales de los 2 centros.
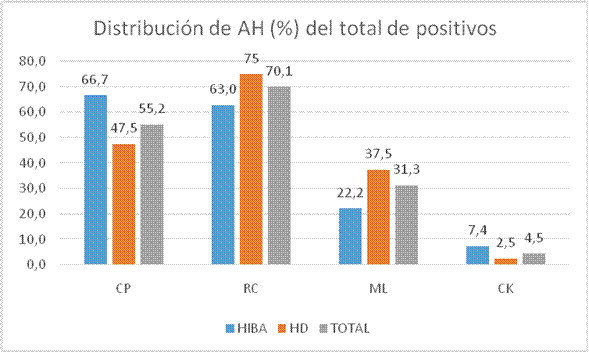
Figura 3.
Distribución porcentual de patrones de anticuerpos heterófilos.
CP, células parietales; RC, ribete en cepillo; ML, músculo liso; CK, células de Kupffer; AH, anticuerpos heterófilos; Total, corresponde al porcentaje del patrón en el total de muestras con presencia de anticuerpos heterófilos; HIBA, Hospital Italiano; HD, Hospital Durand.
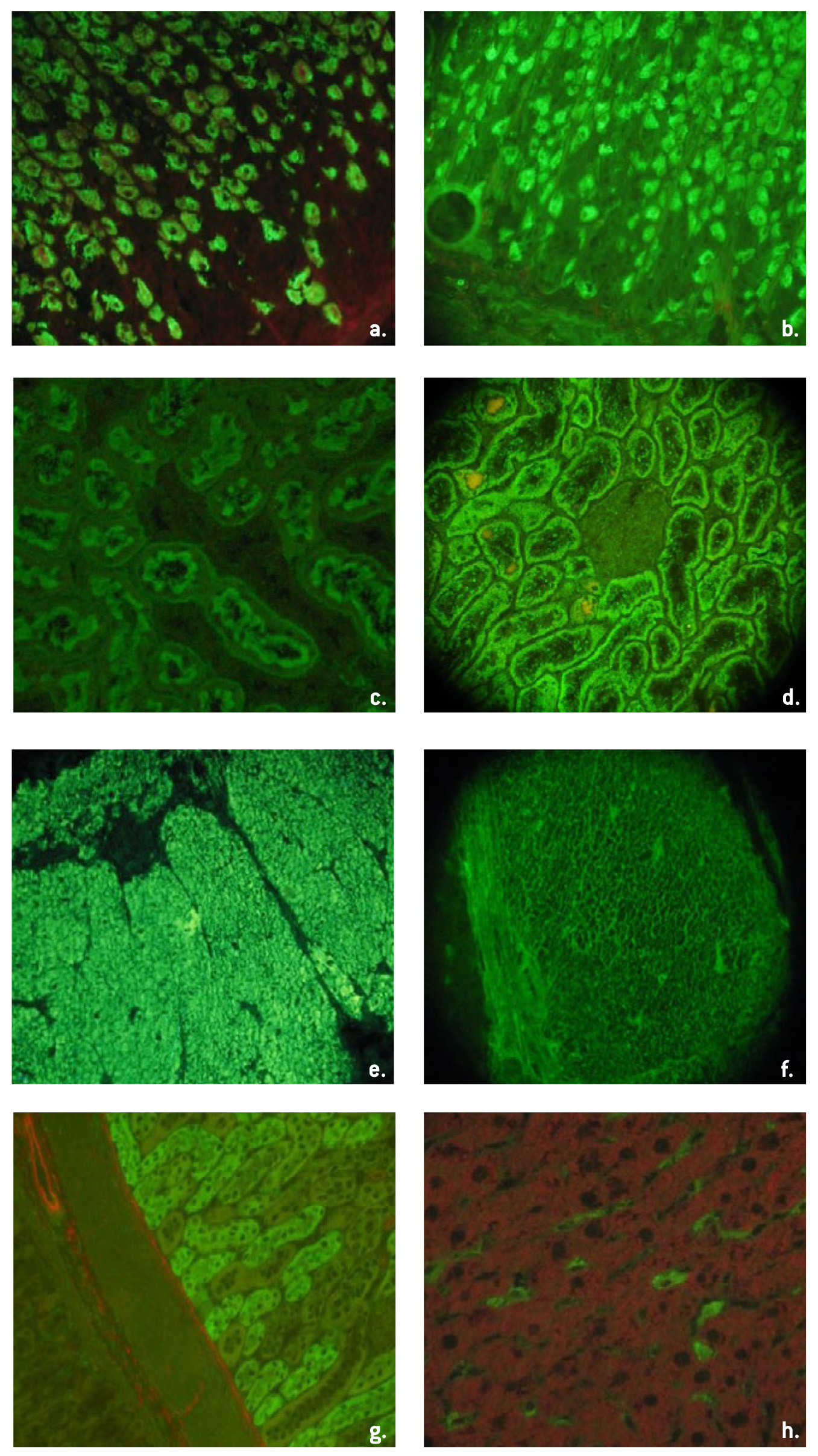
Foto
Cortes criostáticos de 5 mm de espesor, de hígado, riñón y estómago de rata (400X)
a) anticuerpos anticélulas parietales gástricas positivos; b) tinción de las células parietales de las glándulas del estómago por anticuerpos heterófilos; c) anticuerpos antimitocondriales; d) tinción de ribete en cepillo de anticuerpos heterófilos; e) anticuerpos antimúsculo liso; h) AH que tiñen las células de Kupffer; g) anticuerpos anti-LKM; f) anticuerpos heterófilos en músculo liso del estómago.
Discusión
El 19,2 % de las muestras estudiadas presentaron anticuerpos específicos (HIBA: 24 % - HD: 13,7 %) Esta diferencia entre los dos centros, uno privado y el otro público, se puede deber a la diversidad en las poblaciones que asisten a cada centro. (Tabla I). Se observaron diferencias significativas en APCA (p = 0,0338) y en ASMA (p = 0,0081) y no significativas en AMA (p = 0,4026) y LKM (p = 0.5604). (Figura 1). El 10,1 % de los sueros recibidos para estudio de autoanticuerpos fue positivo para AH, con representación de distintos patrones de tinción característicos, que hay que tener en consideración cuando se están estudiando autoanticuerpos. En nuestra serie de pacientes, fue hallado AH en un porcentaje similar al publicado y puede ser mayor en muestras de individuos con historias de aloinmunización.5,6
Se obtuvieron diferencias significativas entre los dos centros en presencia de AH (p = 0,0011), principalmente para ML (p = 0,0350) y para RC (p = 0,0318), mientras que no se encontraron diferencias significativas para CP (p = 0,7578) y para CK (p = 0,5672). (Tabla II). Estas divergencias probablemente se deban a que las poblaciones que asisten a los dos centros pueden ser diferentes, ya que estos anticuerpos se encuentran aumentados en poblaciones con mayor exposición a antígenos, mujeres multíparas o por transfusiones de sangre, en el caso de la aloinmunización. Solo fue investigada la presencia del isotipo IgG de los AH. Según la literatura, en todos los casos, estos anticuerpos son del isotipo IgG y, generalmente, de baja avidez, con actividad multiespecífica. Por otro lado, en el estudio de autoanticuerpos en enfermedades hepáticas y gastrointestinales, los anticuerpos de isotipo IgG son más relevantes y específicos para el diagnóstico que los otros isotipos.5,7
El 3,2 % de las muestras estudiadas mostró una coloración tanto en ML del estómago como de endomisio, que también se puede observar en cortes de corazón de rata.5 Los patrones más comúnmente encontrados en nuestra serie fueron los de CP (5,6 %) y RC (7,1 %). Estos anticuerpos, que fueron caracterizados por Hawkins et al. en 1977, dificultan la interpretación de los patrones de fluorescencia específicos cuando están presentes, ya que pueden enmascararlos y generar resultados falsos negativos.5 Por otro lado, los AH podrían interpretarse como el patrón del anticuerpo de tejido específico, al generar resultados falsos positivos.5,8,11En ninguno de los sueros estudiados, se pudo verificar la presencia de AE cuando estaban presentes los AH. Sin embargo, Scott-Morgan et al. encontraron que el 19 % de los sueros previamente estudiados, en los que no se había detectado la presencia de autoanticuerpos, era positivo después de la eliminación de los AH por técnicas de absorción, si bien solo el 4 % tenía títulos significativos como para ser informados.11
La importancia de este estudio radica en que el patrón que muestran los AH positivos en el hígado podría ser interpretado o confundirse con los anticuerpos antireticulina, los AH que tiñen las CP con APCA o incluso con la reacción positiva que se ve en las CP cuando un AMA está presente. De la misma manera, los AH que tiñen el RC pueden confundirse con AMA y los que colorean el ML, con ASMA. (Foto).12,13,14La interferencia positiva de estos anticuerpos podría evitarse utilizando tejidos de ratón o tejido humano como sustrato.10Sin embargo, si bien los AH no reaccionarían con las CP o RC en tejido de ratón3,4,5, este presenta antígenos heterófilos en el músculo del estómago, que podrían guiar a falsos positivos en ASMA. Por otro lado, la utilización de tejido humano no parece ser una buena elección debido a la necesidad de contar con un laboratorio que pueda procesar este tipo de tejido y hacer las preparaciones. Asimismo, el tejido humano puede presentar aloantígenos de tejidos no específicos que pueden reaccionar con isohemaglutininas presentes en el suero en estudio. Por último, el tejido de rata permite una más fácil manipulación, mayor rendimiento y menor costo. Este tipo de tejidos son los más comúnmente usados en el estudio de anticuerpos de utilidad diagnóstica, por lo que advertimos extremar el cuidado en la interpretación de imágenes obtenidas cuando los AH están presentes para evitar así errores de interpretación que puedan conducir a un diagnóstico equivocado.10,15,16Coincidiendo con la literatura,17 en las muestras estudiadas, los AH fueron encontrados en elevada frecuencia (10,1 %) y hasta con 3 patrones característicos concomitantemente. Por lo tanto, es de suma importancia que el observador esté entrenado para distinguirlos, ya que podrían mimetizar los AE y llevar a una interpretación errónea de los resultados.
Referencias bibliográficas
1. Taber’s cyclopedic medical dictionary. Philadelphia, PA: FA Davis,1989:826. https://fadavispt.mhmedical.com/content.aspx?sectionid=174264026&bookid=2132#174264112
2. Dawkins RL, Stephen C, Pummer B, Romano G, Frueger B, Peter N et al. Heterophile Antibodies. In JB Peter and Y Shoenfeld Editors. Autoantibodies, 1th ed. Netherlands. Elsevier 1996. P351-356.
3. Ireton HJ, Muller HK, McGiven AR. Human antibody against rat gastric parietal cells and kidney brush border. Clin Exp Immunol. 1971;8(5):783-9.
4. Strickland RG, Hooper B. The parietal cell heteroantibody in human sera: prevalence in a normal population and relationship to parietal cell autoantibody. Pathology. 1972;4(4):259-63.
5. Hawkins BR, McDonald BL, Dawkins RL. Characterization of immunofluorescent heterophile antibodies which may be confused with autoantibodies. J Clin Pathol. 1977;30(4):299-307.
6. McDonald BL, Hawkins BR, Dawkins RL, Davey MG. Characterization of human heterophile antibodies apparently induced by alloimmunization. Vox Sang. 1977;33(3):143-9.
7. Kaplan SS Levinson. When is a heterophile antibody not a heterophile antibody? When is it an antibody against a specific immunogen. Clin Chem. 1999;45(5):616-18
8. Van Der Geld H. Anti-Heart Antibodies in The Postpericardiotomy and The Postmyocardial-Infarction Syndromes. Lancet. 1964;2(7360):617-21.
9. Ireton HJ, Muller HK, McGiven AR. Human antibody against rat gastric parietal cells and kidney brush border. Clin Exp Immunol. 1971;8(5):783-9.
10. Strickland RG, Hooper B. The parietal cell heteroantibody in human sera: prevalence in a normal population and relationship to parietal cell autoantibody. Pathology. 1972;4(4):259-63.
11. Scott-Morgan L y Lloyd RS. Problems associated with the presence of immunofluorescent heterophile antibody in sera submitted for autoantibody screening. J. Immunol. Met. 1984;66:69-74.
12. Rizzetto M, Doniach D. Types of 'reticulin' antibodies detected in human sera by immunofluorescence. J Clin Pathol. 1973;26(11):841-51.
13. Doniach D, Roitt IM, Walker JG, Sherlock S. Tissue antibodies in primary biliary cirrhosis, active chronic (lupoid) hepatitis, cryptogenic cirrhosis and other liver diseases and their clinical implications. Clin Exp Immunol. 1966;1(3):237-62.
14. Johnson GD, Holborow EJ, Glynn LE. Antibody to smooth muscle in patients with liver disease. Lancet. 1965;2(7418):878-9.
15. Muller HK, McGiven AR, Nairn RC. Immunofluorescent staining of rat gastric parietal cells by human antibody unrelated to pernicious anaemia. J Clin Pathol. 1971;24(1):13-4.
16. Strickla RG, Hoope B. The parietal cell heteroantibody in human sera: Prevalence in a normal population and relationship to parietal cell autoantibody. Patholoy. 1972;4:259-63.
17. Hawkins BR, Saueracker GC, Dawkins RL, Davey MG, O´Connor KJ. Population Study of Heterophile Antibodies. Vox Sang 1980; 39: 339-342
Notas