Artículos originales
Evaluación de la performance de 4 kits comerciales de testeo rápido antigénico de SARS COV-2 en el diagnóstico de COVID-19.
Evaluation of the performance of kits for rapid antigen testing of SARS-CoV-2 in COVID-19 diagnosis
Evaluación de la performance de 4 kits comerciales de testeo rápido antigénico de SARS COV-2 en el diagnóstico de COVID-19.
Bioquímica y Patología Clínica, vol. 87, núm. 2, pp. 26-31, 2023
Asociación Bioquímica Argentina
Resumen: En el contexto de la pandemia causada por SARS-CoV-2, uno de los puntos fundamentales para controlar la transmisión viral fue el diagnóstico precoz. Por ello, se comercializaron diferentes kits de diagnóstico rápido como el test de antígeno en hisopado nasal o nasofaríngeo. Objetivos: Evaluar el desempeño analítico de cuatro kits de testeo rápido de antígeno de SARS-CoV-2, comparándolos con la reacción en cadena de la polimerasa con transcripción reversa en tiempo real (RT-qPCR) como método de referencia. Materiales y métodos: Se analizaron los resultados de cuatro kits de test rápido de antígeno realizados en muestras de hisopado nasal o nasofaríngeo, de acuerdo con el kit, de pacientes que concurrieron a la Unidad Febril de Urgencia del Hospital Durand entre julio de 2021 y febrero de 2022, comparándolos con los resultados obtenidos simultáneamente por RT-qPCR en hisopado nasofaríngeo. Resultados: En su totalidad, fueron analizadas 13735 muestras. Se obtuvieron los siguientes valores de sensibilidad, especificidad, valor predictivo positivo y negativo, respectivamente, para: Panbio™ COVID-19 Ag Abbott hisopado nasofaríngeo: 56,41 %, 99,92 %, 98,60 % y 95,65 %; Panbio™ COVID-19 Ag Abbott hisopado nasal: 65,20 %, 100 %, 100 % y 98,80 %; COVID-19; Juschek hisopado nasal: 77,89 %, 99,30 %, 93,09 % y 97,39 %; GeneFinderTM COVID-19 Ag Plus hisopado nasofaríngeo: 78,21 %, 99,57 %, 97,90 % y 100 %. Conclusiones: Los cuatro kits evaluados tienen una performance similar, con resultados óptimos de especificidad, valor predictivo positivo y negativo. La sensibilidad en la población evaluada es menor que la reportada por los fabricantes y presenta diferencias estadísticamente significativas entre los diferentes kits.
Palabras clave: COVID-19, infección por SARS-CoV-2, transmisión, diagnóstico precoz.
Abstract: In the context of the pandemic caused by SARS-CoV-2, one of the key points to control disease spread was early diagnosis. Thus, several rapid diagnostic kits, such as nasopharyngeal and nasal antigen tests, were commercialized. Objectives: To evaluate the performance of four SARS-CoV-2 rapid antigen test kits, comparing them with the Real-time Reverse Transcription-Polymerase Chain Reaction (RT-qPCR), as the gold standard method. Materials and methods: Results from four rapid test kits performed on nasal or nasopharyngeal swabs from patients who attended the Febrile Urgent Unit of Durand Hospital (Buenos Aires, Argentina) between July 2021 and February 2022 were analyzed and compared with RT-qPCR in nasopharyngeal swabs. Results: A total of 13735 samples were analyzed. The sensitivity, specificity, and positive and negative predictive values of each test were as follows: Panbio™ COVID-19 ANTÍGENO ABBOTT in nasopharyngeal swab: 56.41%, 99.92%, 98.60% and 95.65% respectively; Panbio™ COVID-19 ANTÍGENO ABBOTT in nasal swab: 65.20%, 100%, 100% and 98.80% respectively; COVID-19 JusChek in nasal swab: 77.89%, 99.30%, 93.09% and 97.39% respectively; and GeneFinder™ COVID-19 Ag Plus in nasopharyngeal swab: 78.21%, 99.57%, 97.90% and 100% respectively. Conclusions: The performances for the four kits were similar and had optimal specificity, and positive and negative predictive values. The sensitivity values in the study group were lower than the ones specified by the manufacturer with statistically significant differences.
Keywords: COVID-19, SARS-CoV-2 infection, transmission, early diagnosis.
Introducción
Los coronavirus son un grupo diverso de virus envueltos con un genoma de ARN monocatenario de sentido positivo, que pertenecen a la familia Coronaviridae. En diciembre de 2019, surgió en la población humana un nuevo betacoronavirus, el SARS-CoV-2 (coronavirus-2 del síndrome respiratorio agudo severo), responsable de la enfermedad COVID-19. Debido a la alta transmisibilidad y rápida propagación global de este virus1, la Organización Mundial de la Salud declaró la pandemia de COVID-19 en marzo de 2021. Su cuadro clínico comprende un amplio conjunto de signos y síntomas que van desde fiebre, tos, odinofagia, cefalea, mialgia, diarrea/vómitos, rinitis/congestión nasal y/o disgeusia/anosmia hasta cuadros más graves con neumonía y dificultad respiratoria con necesidad de hospitalización y riesgo de muerte.2 El diagnóstico precoz se tornó clave para el rápido aislamiento de aquellos individuos infectados, con el objetivo de reducir la transmisión persona-persona.3
La definición de caso sospechoso requiere como primer criterio la presencia de 2 o más síntomas determinados, sin otra causa o etiología aparente, o 1 síntoma, para grupos considerados de alto riesgo. A lo largo del tiempo, fueron incorporándose síntomas a la definición hasta llegar al listado descrito anteriormente; se incorporó la pérdida de gusto/olfato como posible único síntoma, y se consideraron como grupos de alto riesgo el personal esencial y personas que habitan en barrios populares, entre otros.4,5
Para el diagnóstico de COVID-19, el método de referencia es la detección del ácido ribonucleico (ARN) viral mediante la reacción en cadena de la polimerasa con transcripción reversa en tiempo real (RT-qPCR). A fin de lograrlo, se dispone de diversos kits comerciales y se requiere de un laboratorio de complejidad media - alta y personal profesional capacitado. El tiempo de respuesta de RT-qPCR puede variar entre 12 - 72 horas, según la capacidad operativa de la institución, que incluye desde el pre procesamiento de la muestra y el tiempo analítico de la propia PCR hasta la ulterior digitalización de los resultados. Para aumentar la capacidad operativa con técnicas de menor complejidad y diagnóstico rápido, se incorporó a la práctica diaria el test rápido de antígeno de SARS-CoV-2. Estos tests son tradicionalmente utilizados para tamizaje, por lo que deben tener una alta sensibilidad, bajo porcentaje de falsos negativos y alto valor predictivo negativo, con el objetivo de detectar rápidamente la mayor cantidad posible de individuos infectados, favorecer la búsqueda oportuna de contactos y así disminuir la propagación viral. Son inmunoensayos cromatográficos que, generalmente, tienen un principio de detección de tipo sándwich en un formato de ensayo de flujo lateral que permiten la detección cualitativa de proteínas virales6 y pueden presentar tres resultados posibles: positivo (banda que indica la presencia de antígeno de SARS-CoV-2 y banda correspondiente al control interno), negativo (solo se observa la banda correspondiente al control interno) o inválido (cuando no se observa banda control). Estos test se utilizan como point of care tests (POCT) en las Unidades Febriles de Urgencia (UFU) de los hospitales públicos de la Ciudad Autónoma de Buenos Aires, desde enero de 2021. El tiempo analítico es de aproximadamente 30 minutos, con tiempos de entrega de resultados positivos de 2 a 3 horas, por lo que se cumple el principal objetivo, que es el diagnóstico rápido. Los resultados negativos se confirmaron por RT-qPCR,según el algoritmo de GCBA, hasta marzo de 2022.7
Desde su implementación en enero de 2021, el Gobierno de la Ciudad de Buenos Aires proveyó de insumos a los diferentes hospitales, cambiando de kits según su disponibilidad en Argentina y su adjudicación por licitaciones públicas. Esto hizo necesaria la rápida evaluación de cada nuevo kit disponible. Por otro lado, los datos aportados por los respectivos fabricantes indican que los resultados positivos correlacionan con RT-qPCR detectables con Ct (cycle threshold o ciclo umbral) menores que 25, entendiéndose de forma convencional el Ct como el ciclo a partir del cual la fluorescencia supera el umbral de ruido y tiene una relación inversamente proporcional con la cantidad de ARN target presente en la muestra.
El objetivo de este trabajo fue evaluar la performance de cuatro kits de test rápido de antígeno utilizados por el laboratorio del Hospital General de Agudos “Dr. Carlos G. Durand" de la Ciudad Autónoma de Buenos Aires mediante el análisis de sensibilidad, especificidad, valor predictivo positivo y valor predictivo negativo, utilizando la RT-qPCR como método de referencia. Además, se analizó el porcentaje de falsos negativos y verdaderos positivos para muestras con RT-qPCR con Ct menores que 25.
Materiales y métodos
Se realizó un estudio analítico, de corte transversal, en diferentes períodos comprendidos entre julio de 2021 y febrero de 2022, en el cual se incluyeron pacientes que ingresaban a la UFU del Hospital Durand por demanda espontánea, que cumplían la definición vigente de caso sospechoso, con síntomas leves o moderados. En el período de diciembre a febrero se incluyeron, además, pacientes asintomáticos, según modificaciones en la normativa vigente. A cada paciente, se le tomaron 2 muestras simultáneas, una de hisopado nasal (HN) o nasofaríngeo (HNF) para el test rápido (según el kit disponible en cada momento) y la otra de hisopado nasofaríngeo para la realización de la RT-qPCR. Todos los resultados del test rápido de antígeno, en los períodos evaluados, fueron confirmados por RT-qPCR.
Durante el estudio, se utilizaron cuatro kits de test rápido de antígeno que detectan la nucleoproteína (N) viral, sujetos a la disponibilidad de entrega por parte del Ministerio de Salud. A continuación, se detallan los test rápidos de antígeno utilizados, el tipo de muestra requerida, los períodos en que fueron evaluados y la sensibilidad (S) y especificidad (E) reportadas por los fabricantes:
1) Test rápido Panbio™ COVID-19 Ag Abbott en hisopado nasofaríngeo, desde el 31/07/2021 a 11/08/2021 (S 91,40 %; E 99,80 %);
2) Test rápido Panbio™ COVID-19 Ag Abbott en hisopado nasal, del 12/08/2021 al 10/11/2021 (S 91,10 %; E 99,70 %);
3) Test rápido de antígeno COVID-19 Juschek en hisopado nasal, desde el 10/11/2021 al 10/12/2021 (S 93,6 %; E >99,90 %);
4) Test Rápido GeneFinderTM COVID-19 Ag Plus en hisopado nasofaríngeo, desde el 17/02/2022 al 24/02/2022 (S 94,95 %; E 98,00 %).
Paralelamente, se relevó la tasa de positividad diaria de muestras provenientes de la UFU durante todo el período de utilización del algoritmo de test rápido y se confirmó por RT-qPCR.
Se excluyeron del análisis los test rápidos inválidos y los hisopados nasofaríngeos para RT-qPCR que, por distintos motivos, no fueron recibidos o fueron mal remitidos al laboratorio.
Todas las muestras para RT-qPCR fueron analizadas en el Laboratorio de Biología Molecular del Hospital Durand de la Ciudad Autónoma de Buenos Aires. Los kits utilizados para la extracción de ácidos nucleicos de las muestras estudiadas fueron MPure Viral/Pathogen Nucleic acid extraction Kit B-Mpure System y MagaBio Plus virus DNA/RNA extraction kit III-Bioer, en tanto que para la RT-qPCR se emplearon: DisCoVery SARS-CoV-2 RT-PCR Detection Kit Rox/Cy5. WGene SARS-CoV-2 RT Detection. SARS-CoV-2 ELITe MGB® Kit y por último RealStar® SARS-CoV-2 RT-PCR Kit 1.0. Estos métodos se consideran de desempeño equivalente en estudios previamente publicados por Fellner y col.8 y en estudios comparativos realizados en nuestro laboratorio, previa implementación.
Se llevó a cabo el cálculo de sensibilidad, especificidad, valor predictivo positivo y valor predictivo negativo para cada kit. El intervalo de confianza se calculó mediante aproximación normal/método asintótico y el análisis de proporción poblacional para muestras grandes. Para comparar globalmente las sensibilidades obtenidas en los diversos kits se utilizó el método de chi cuadrado y para la comparación individual, el test de diferencia de proporciones con la corrección de Bonferroni.
Resultados
En su totalidad, fueron analizadas 13735 muestras de pacientes que comprenden 5661 hombres y 8074 mujeres entre 1 y 99 años de edad. La cantidad de test de antígeno realizados con cada kit y los resultados positivos, negativos e inválidos, así como también los resultados falsos positivos y negativos asociados a cada kit, se resumen en la Tabla I.
En la Figura 1, se muestra el período de evaluación de cada kit de test de antígeno en relación con el número de muestras positivas (sumatoria de test de antígeno y RT-qPCR) y el número de muestras analizadas totales, y la tasa de positividad global de nuestro hospital (sumatoria de test de antígeno y RT-qPCR), en cada semana epidemiológica.
En la Tabla II, se resumen los resultados de sensibilidad, especificidad, valores predictivos positivo y negativo y sus respectivos intervalos de confianza, del 95 %, para cada kit.
Por otro lado, en la comparación global de sensibilidades, se obtuvo un p=0,0002, mientras que en todas las comparaciones individuales el p obtenido fue de <0.05.
La Figura 2 muestra la cantidad de falsos negativos y verdaderos positivos obtenidos para los distintos kits de test de antígeno, agrupados de acuerdo con el rango de Ct obtenido en la RT-qPCR. El porcentaje de falsos negativos con Ct menores que 25 fluctuó entre un 9 % y un 12 %. Por otro lado, en relación con los verdaderos positivos de test de antígeno, con Ct mayores que 25, el porcentaje varió entre un 9 % y un 29 %.
| Muestra | Test | TA Realizados (N) | TA Positivos (N) (%) | TA Negativos (N) (%) | TA Inválidos (%) | Falsos positivos (%) | Falsos negativos (%) | |
| HNF | Panbio™ COVID-19 Ag Abbott | 1238 | 23 (1,86 %) | 1215 (98,14 %) | 0 (0 %) | 1 (4,35 %) | 17 (1,40 %) | |
| GeneFinderTM COVID-19 Ag Plus | 878 | 143 (16,29 %) | 735 (83,71 %) | 0 (0 %) | 3 (2,1 %) | 39 (5,3 %) | ||
| HN | Panbio™ COVID-19 Ag Abbott | 8869 | 197 (2,22 %) | 8643 (97,45 %) | 29 (0,33 %) | 0 (0 %) | 103 (1,19 %) | |
| Test rápido de antígeno COVID-19 Juschek | 2750 | 246 (8,95 %) | 2494 (90,69 %) | 10 (0,36 %) | 18 (7,32 %) | 66 (2,65 %) |
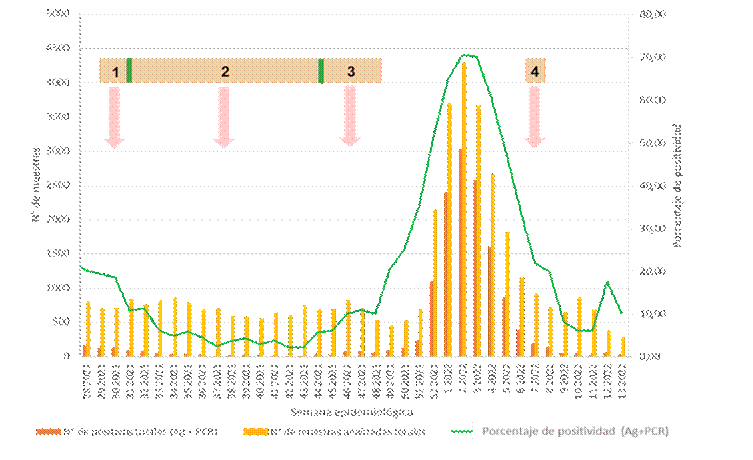
Figura 1.
Tasa de positividad en la UFU del Hospital “Carlos G. Durand”, según semana epidemiológica y período de evaluación de cada kit de test de antígeno.
1, Abbott HNF; 2, Abbott HN; 3, Juschek HN; 4, GeneFinder HNF.
| Test | Sensibilidad % (IC%) | Especificidad % (IC%) | Valor predictivo positivo % (IC%) | Valor predictivo negativo % (IC%) | |
| Panbio™ COVID-19 Ag Abbott HNF | 56,41 (40,85-71,97) | 99,92 (99,75-100,08) | 95,65 (87,32-103,99) | 98,60 (97,94-99,26) | |
| GeneFinderTM COVID-19 Ag Plus | 78,21 (72,16-84,26) | 99,57 (99,09-100,06) | 97,90 (95,55-100,25) | 94,69 (93,07-96,31) | |
| Panbio™ COVID-19 Ag Abbott HN | 65,20 (59,78-70,63) | 100 (100-100) | 100 (100-100) | 98,80 (98,58-99,04) | |
| Test rápido de antígeno COVID-19 Juschek | 77,55 (72,78-82,32) | 99,26 (98,93-99,60) | 92,68 (89,43-95,94) | 97,35 (96,72-97,98) |
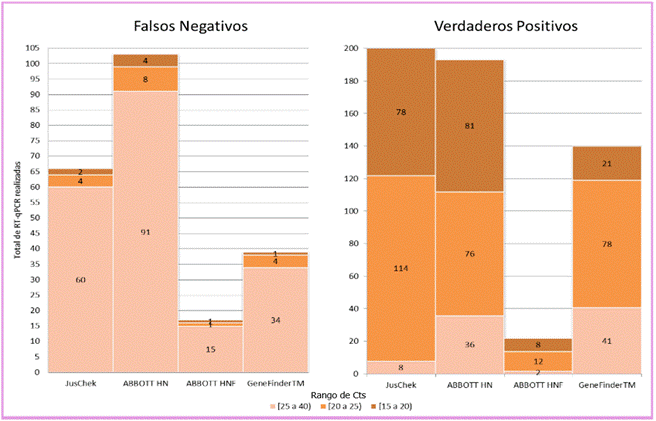
Figura 2.
Falsos negativos y verdaderos positivos agrupados de acuerdo con el rango de Ct obtenido en la RT-qPCR.
Ct, cycle thershold; HNF, hisopado nasofaríngeo; HN, hisopado nasal.
Discusión
Los test rápidos evaluados resultaron tener una performance comparable, con alta especificidad y óptimos valores predictivos tanto positivo como negativo. Sin embargo, si bien la sensibilidad para la población evaluada en el período de tiempo analizado resultó aceptable, fue menor que la reportada por los fabricantes, con diferencias estadísticamente significativas tanto en forma global como individual, con una probabilidad de error menor de 5 %.
En un metaanálisis realizado por Valentin Parvu y col.9, en el que se analizan 83 estudios que comparan la performance del test rápido de antígeno con la RT-qPCR, se observó un amplio grado de heterogeneidad entre los valores de sensibilidad obtenidos en los distintos trabajos, con un promedio de 75 % (71 %-78 %), que se asemeja al obtenido en dos de los cuatro kits analizados en este trabajo (GeneFinderTM COVID-19 Ag Plus y test rápido de antígeno COVID-19 Juschek). No obstante, la sensibilidad de los otros dos kits evaluados (Panbio™ COVID-19 Ag Abbott HN y Panbio™ COVID-19 Ag Abbott HNF) resultó más cercana a 56 %, que es la obtenida en el estudio de Jacqueline Dinnes y col.10 Por otra parte, teniendo en cuenta que el personal encargado de la toma de muestras sufrió un alto recambio en el transcurso del tiempo y que, consecuentemente, requerían cierto tiempo de capacitación y práctica, es posible que una de las causas asociadas a la sensibilidad obtenida sea una incorrecta toma de muestras, como también, la heterogeneidad de las muestras respiratorias, lo cual podría favorecer la aparición de resultados falsos negativos en el test de antígeno. El factor de agotamiento del personal, asociado al gran volumen de pacientes atendidos, a las largas jornadas de trabajo y al estrés físico y mental influye en la etapa preanalítica y analítica.
A pesar de lo mencionado previamente, si se tuvieran en cuenta solo los resultados de test rápido de antígeno, cuyos Ct por RT-qPCR resultaron menores que 25, el valor de falsos negativos disminuiría notoriamente.
Por otro lado, no se observaron diferencias marcadas en la performance de aquellos test de antígeno que utilizaron como muestras hisopados nasofaríngeos y los que utilizaron hisopados nasales.
Teniendo en cuenta la existencia de distintos tipos de pruebas disponibles para el diagnóstico de COVID-19, es importante resaltar que su interpretación debe ser realizada de acuerdo con el contexto epidemiológico en que son utilizadas. En los distintos períodos de tiempo incluidos en este estudio, la tasa de positividad global del hospital fluctuó entre 4 % y 20 %. Para poder realizar una comparación óptima, sería ideal poder analizar los distintos kits en un mismo período de tiempo y en las mismas condiciones respecto de la prevalencia de la enfermedad, estacionalidad y cepa circulante predominante. Sin embargo, esto es utópico, ya que una característica de la pandemia por COVID-19 ha sido el alto dinamismo epidemiológico, con surgimiento de nuevas variantes de mayor transmisibilidad. A su vez, la industria biomédica fue incorporando diferentes ensayos a lo largo del tiempo. En ese contexto, la evaluación de cada test rápido in situ y en el momento de su incorporación fue valiosa para conocer el comportamiento de los ensayos utilizados.
El uso del test de antígeno fue una herramienta destacada en la pandemia que permitió, por un lado, la toma de decisiones rápidas para el diagnóstico oportuno de COVID-19 y, por otro, descomprimió el trabajo en los laboratorios de Biología Molecular, colaborando, en ciertos períodos de la pandemia, en el control y disminución del flujo de RT-qPCR.
Agradecimientos
Agradecemos a todo el personal del Laboratorio del Hospital General de Agudos “Dr. Carlos G. Durand” y, en especial, al Bioq. Sergio Santiago y a los que forman parte de las áreas de Biología Molecular, Epidemiología y de la Unidad Febril de Urgencia por el apoyo para la realización de este trabajo.
Referencias bibliográficas
1. Paules CI, Marston HD, Fauci AS. Coronavirus Infections-More Than Just the Common Cold. Journal of the American Medical Association. [internet] 2020. p. 707-8. Disponible en: https://jamanetwork.com/journals/jama/article-abstract/2759815
2. Ministerio de Salud de la Nación [sede web]. Argentina; 2020 [acceso 21 de enero de 2022]. Definiciones y clasificaciones de caso. Disponible en: https://www.argentina.gob.ar/salud/coronavirus/definicion-de-caso
3. Rearte Analía, Giovacchini Carlos, Voto Carla, Baumeister Elsa, Pifano Marina, Fischerman Laura, et al. Consenso sobre el uso de pruebas diagnósticas para SARS-CoV-2-Versión 2. Ministerio de Salud [internet]. 3 de mayo de 2021. Disponible en: https://bancos.salud.gob.ar/sites/default/files/2021-06/CONSENSO_Diagnostico_SARS_CoV-2_Actualizacion_Mayo_2021.pdf
4. Gobierno de la Ciudad de Buenos Aires [sede web]. Protocolo de manejo de casos sospechosos y confirmados COVID-19 en aislamiento en instituciones extrahospitalarias. Mayo 2021. Disponible en: https://www.buenosaires.gob.ar/sites/gcaba/files/id_2ab_-_protocolo_de_manejo_de_casos_sospechosos_y_confirmados_covid-19_en_aislamiento_en_instituciones_extra-hospitalarias_1.pdf
5. Gobierno de la Ciudad de Buenos Aires [sede web]. Protocolo de manejo de casos sospechosos y confirmados de COVID-19. Versión 49. 30/12/21. Disponible en: https://www.buenosaires.gob.ar/sites/gcaba/files/id_0_-_protocolo_de_manejo_frente_a_casos_sospechosos_y_confirmados_de_covid-19_30.12.pdf
6. Gobierno de la Ciudad de Buenos Aires. Protocolo operativo. Test de antígeno COVID-19. [sede web]. Argentina. 2022. [actualizada 2022; acceso 1 de abril de 2022].
7. Gobierno de la Ciudad de Buenos Aires. Protocolo operativo-Versión 3. Test de antígeno COVID-19. [sede web]. Argentina. 2021. [actualizada 2022; acceso 23 de diciembre de 2021].
8. Fellner MD, Bonaventura R, Basiletti J, Avaro M, Benedetti E, Campos A, et al. Evaluation of RT-qPCR and Loop-Mediated Isothermal Amplification (LAMP) Assays for the Detection of SARS-CoV-2 in Argentina. Genes (Basel). 2021;12(5): 659.
9. Parvu V, Gary DS, Mann J, Lin YC, Mills D, Cooper L, et al. Factors that Influence the Reported Sensitivity of Rapid Antigen Testing for SARS-CoV-2. Front Microbiol. 2021;12:714242.
10. Dinnes J, Deeks JJ, Adriano A, Berhane S, Davenport C, Dittrich S, et al. Rapid, point-of-care antigen and molecular-based tests for diagnosis of SARS-CoV-2 infection. Cochrane Database Syst Rev. 2020;8(8):CD013705.
Notas